
Önemli Gelişme – Kanser Hücresinin Temel Özellik Sayısı 14 Oldu
"Kanser hücrelerini normal hücrelerden ayıran temel farklar nedir?" sorusuna ilk kapsamlı cevap 2000 yılında gelmişti ve normal hücrelerin çok aşamalı bir süreçte kanserleşmesinin 6 temel özelliği tanımlanmıştı.
Bu 6 özelliğe "Hallmarks of Cancer Cells" dendi ve sonraki yıllarda bu özelliklere 4 yeni özellik daha eklenmiş ve karmaşık süreç biraz daha aydınlatılmıştı. 2022 yılında ise kanserin 10 temel özelliğine 4 yeni özellik daha eklendi. Artık kanserin bildiğimiz 14 temel özelliği var.
Bilim insanları bu haberi coşku ile karşıladı. Birçok bilim insanı da kendi çalışma alanlarının kanser biyolojisinin temel özellikleri arasında kabul edildiğini görmenin heyecanını Twitter’dan paylaştı.
2000 yılında yayımlanan ilk orijinal makalede kanser araştırmalarının öncülerinden Whitehead Biyomedikal Araştırma Enstitüsü ve Massachusetts Teknoloji Enstitüsü’nden "Robert Weinberg" ve İsveç Federal Teknoloji Enstitüsün’den "Douglas Hanahan", kanser hakkındaki en son yayımlanan bilgileri, insan kanserlerinin tümü olmasa da çoğu tarafından paylaşılan temel özellikler olarak, hastalığın olağanüstü karmaşıklığını özetleyen mantıksal bir çerçevede düzenlediler.
Douglas Hanahan, sonraları "Kanserin Temel Özellikleri" ile özdeşleşen isim oldu. Bir dönüm noktası olarak kabul edilen Kanserin Temel Özellikleri çalışması, kanser biyolojisini anlamak ve incelemek için kapsamlı bir temel sağlayarak kısa sürede kanser araştırmacıları tarafından önemli bir kaynak haline geldi. Devam eden yıllarda ise kanserin temel özelliklerine yenileri eklendi.
Günümüzde kanser ilaçları, kanserin temel özellikleri hedeflenerek geliştirilmektedir.
2000 – Kanserin Bilinen İlk Temel Özellikleri

İlk düzenlemede kanserin 6 temel özelliği bildirildi;
- Büyüme sinyallerinde kendi kendilerine yetme: Normal hücreler, çoğalma için dış büyüme sinyallerine bağlıyken kanser hücreleri, dış uyarıcılara bağlılıklarını büyük ölçüde azaltabilir veya yok edebilirler ve böylelikle çoğu büyüme sinyallerini kendi kendilerine üretebilir. Ayrıca daha sonra, kanserin hücrelerinin çevredeki normal hücreleri, pasif seyirciler yerine aktif işbirlikçiler olarak hizmet ettirerek gerekli büyüme sinyallerini sağlaması için etkisi altına alan kompleks dokular olduğu bulundu.
- Büyüme baskılayıcı sinyallerden kaçma: Çoklu çoğalma karşıtı sinyaller, hücreleri, hücre döngüsü dışına ve geçici dinlenme durumuna iterek ya da onları farklılaşma durumuna göndererek, normal dokularda iç-dengeyi sürdürür. Kanserleşme sürecindeki hücreler, hücre döngüsü sürecini kontrol eden mekanizmaları altüst ederek bu çoğalma karşıtı sinyallerden kaçarlar – örneğin; pRb yolunu bozarak ve c-myc gibi büyüme uyarıcı faktörleri aşırı derecede ifade ederek.
- Doku invazyonu ve metastazı aktifleştirme: Metastaz, kansere bağlı yaşam kayıplarının %90'dan fazlasının nedenidir. Uzak dokuları istila etme, yerleşme ve büyüme yeteneği bu nedenle kanserin temel özelliklerinden biridir ve bu, kanser hücresinin e-kadherin, integrinler ve diğer adezyon/yağışma molekülleri aracılığı ile çevreleriyle etkileşimlerindeki değişikliklere ve matrisi parçalayan proteazların üretimine dayanır (İnvazyon, tümörün, başladığı yerden dokunun derinliklerine doğru yayılmasını ifade eder).
- Sınırsız çoğalma potansiyelini açığa çıkarma: Tümörün büyümesi için, kanser hücrelerinin süresiz olarak çoğalması gerekir. Normal hücreler sınırlı bir çoğalma potansiyeline sahipken ve laboratuvarda kültürlenirlerse bir noktada bölünmeyi durdururken, kanser hücreleri telomer kısalması tarafından yönetilen bu kısıtlama mekanizmasını kaybetmiştir. Ölümsüz olmak için kanser hücreleri, telomerlerinin uzunluğunu, bölünmeye devam etmelerini sağlayan kritik bir eşiğin üzerinde tutmak için telomeraz enzimine güvenirler.
- Yeni damar oluşumunu tetikleme (anjiyogenez): Büyüyen tümör dokusunun oksijen ve besin ihtiyaçları artar. Bu nedenle, büyümeye devam etmeleri için pro-anjiyojenik (yeni damar oluşumunu tetikleyici) sinyaller vererek kendileri için yeni damarlar oluşturmaları gerekir. Yazarlar bu özelliği tanımladıklarında, tümörlerin mikroskobik lezyonlardan makroskopik lezyonlara büyümelerine izin veren bir "anjiyojenik anahtardan" geçtiği tespit edilmişti.
- Programlanmış hücre ölümüne karşı direnç geliştirme: Ölümsüz olmak, kanser hücrelerinin sayıca artmaya devam etmesinin başka bir yolu olduğu için apoptoz (programlı hücre ölümü), önemli bir anti-kanser bariyerdir ve kanser hücreleri apoptoz mekanizmalarından kaçabilmektedir. Kanser araştırmacıları, programlı hücre ölümü mekanizmalarını, yeni ilaç keşifleri için yoğun bir şekilde denemektedir.
2011 – Kanserin Temel Özellikleri 10’a Yükseldi
2011 yılında Weinberg ve Hanahan, 2000 yılında yayımlanan kanserin 6 ayırt edici özelliği sayesinde 10 yıl boyunca alınan ilerlemeye yönelik bir yayın yaptı. Ayrıca bu yayında, kanseri açığa çıkan iki yeni temel özelliğini de duyurdular:
- Enerji metabolizmasının yeniden programlanması: Normal hücreler enerji üretmek için glikozu ve oksijeni kullanırken kanser hücreleri, oksijen varlığında bile aerobik glikolize (oksijensiz enerji üretimi) geçebilirler ki bu Warburg etkisi olarak biliniyor. Bu mekanizma daha az verimli olmasına rağmen, daha hızlıdır ve hızlı çoğalmalarını desteklemek adına proteinleri, DNA’yı ve yağları oluşturmak için yapı taşları olarak kanser hücreleri tarafından kullanılan birkaç ara öncülden kaynaklanır.
- Bağışıklık sisteminden kaçma: Günümüzde kanser hücresinin en çok konuşulan ve araştırılan özelliği, bağışıklık sisteminden kaçmak için ustaca kullandığı yöntemlerdir. Kanser hücrelerinin bağışıklık sisteminden saklanmasını engelleyen veya tersi ifade ile, bağışıklık sistemini kansere karşı aktifleştiren ilaçlara immünoterapi diyoruz. Hanahan ve Weinberg, bağışıklığı sıfırlanmış farelerde – özellikle sitotoksik ve yardımcı T hücreleri veya doğal öldürücü hücrelerden yoksunlarsa – kanserlerin daha hızlı büyüdüğünü gösteren fare modellerinde yapılan çalışmalar ve yüksek bağışıklık infiltrasyonu olan insan tümörlerinin daha iyi hastalık gidişatına sahip olduğuna dair gözlemler dahil olmak üzere, bağışıklık sisteminin tümör oluşumuna bir engel olarak oynadığı merkezi rolü destekleyen kanıtları inceledi.
- Kanserleşmeyi destekleyen iltihaplanma (yangı = enflamasyon): 2011 yılında ayrıca tümörü teşvik eden inflamasyonu da yeni bir etkinleştirici özellik olarak tanımladılar. Bağışıklık sistemi hücrelerin tümöre infiltrasyonu, tarihsel olarak bağışıklık sisteminin tümöre karşı tepki gösterdiğinin bir işareti olarak kabul edilirken ikinci yayımda, belirli inflamatuar hücrelerinin tümörü teşvik edici etkisi netleşmiştir. İnflamasyonun büyüme, hayatta kalma ve proanjiyogenik faktörler sağlayarak ve yakındaki kanser hücrelerinde ek mutasyonlara neden olabilecek reaktif oksijen türleri gibi kimyasalları serbest bırakarak birçok ayırt edici özelliği nasıl desteklediği de incelendi. Ek olarak, geçen on yılda bir tümörün biyolojisini incelerken hem kanser hücrelerini hem de etraflarında oluşturdukları mikroçevreyi göz önünde bulundurmak gerektiğini gösteren kapsamlı araştırmaların konusu haline gelen tümör mikroçevresi (TMÇ) hakkında bir paragrafa da yer verildi.
- Genomik kararsızlık ve biriken mutasyonlar: DNA hasarlarının birikmesi kanserleşmenin en önemli sebebidir. Aynı zamanda DNA tamirinde görev alan enzimlerin fonksiyonlarının kaybolması gen yapısındaki bozulmaların artmasını destekler.
2022 – Kanser Biyolojisinin Sınırları Genişliyor: Yeni Temel Özellikler
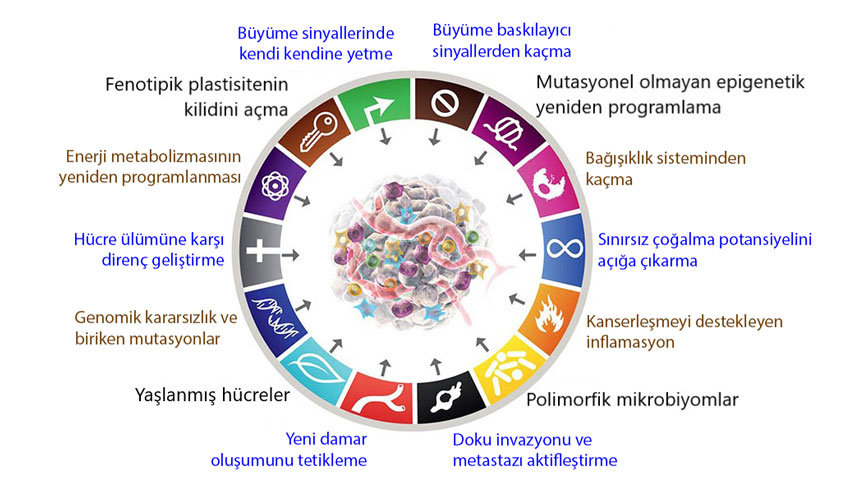
10 yıl sonra Hanahan, büyük veriler aracılığıyla kanser araştırmalarında kaydedilen büyük ilerlemeleri göz önünde bulundurarak ve yeni keşifleri kavramsallaştırmada kanserin ayırt edici özelliklerinin etkisini yeniden teyit ederek ve “bu karmaşıklığı giderek daha mantıklı bir bilim haline getirmeye yardımcı olmak” adına bir kez daha kanserin ayırt edici özellikleri üzerine yoğunlaştı. Yayımlanan son makalede son 10 yılda yapılan araştırmalar, kanserde metabolik yeniden programlamanın ve bağışıklık sistemi yıkımından kaçınmanın önemini büyük ölçüde doğruladığı için, 2011'de ortaya çıkan iki ayırt edici özellik kesin bir şekilde temel özellikler olarak belirlendi. Buna ek olarak, Hanahan ortaya çıkan yeni temel özellikler öneriyor:
- Fenotipik plastisite ve bozulmuş farklılaşma: Normal hücrelerin terminal/uç farklılaşması, çoğalmanın kalıcı bir şekilde durması ile ilişkilidir ve giderek artan kanıtlar, kanser hücrelerinin farklılaşmadan kaçtığını ve büyümeye devam etmek için "fenotipik plastisite" olarak bilinen şeyin kilidini açtığını göstermektedir. Başka bir deyişle, kimliklerini çoğalmaya daha meyilli bir şeye dönüştürebiliyorlar. Bu farklı şekillerde olabilir:
- Tam farklılaşmaya yaklaşan hücreler, geri farklılaşabilirler.
- Farklılaşmamış bir hücreden kaynaklanan kanser hücreleri, farklılaşma sürecini durdurabilir ve kısmen farklılaşmış, kök hücre benzeri durumda kalabilirler.
- Belirli bir farklılaşma tipine bağlı hücreler, gelişimsel programları değiştirebilir veya farklılaşarak kök hücreleriyle ilişkili olmayan özellikler edinebilirler.
Hanahan, diğer ayırt edici özelliklerin geçerli olduğu gibi hücresel plastisite, kanser hücrelerinin "yeni bulduğu bir şey" değildir, aksine bazı normal hücrelerin normal dokuları onarmak ve yenilemek için aktif edebileceği mevcut mekanizmalar üzerinde yapılan kanserle ilişkili değişikliklerdir diyor.
- Mutasyonel olmayan epigenetik yeniden programlama: Epigenetik, genetiğin ötesinde anlamına gelir ve genlerin nasıl davrandıklarını, düzenlendiklerini inceler. Epigenetik mekanizmalar, DNA ve gen yapısında değişikliğe neden olmazlar ancak genin aktif olup olmayacağını belirlerler, yani mutasyon olmadan genetik ifade değişir. Epigenetik değişikliklerin en bilinenleri DNA metilasyonu ve histon modifikasyonudur. Epigenetik manzaradaki global değişiklikler, gerçekten de birçok kanserin yaygın bir özelliği olarak kabul edilmektedir. Kanser hücreleri, gelişmelerini desteklemek için, epigenetik mekanizmalar üzerinden gen ağını yeniden programlayabilirler.
- Mikrobiyom: Vücudumuz, içimizde ve üzerimizde yaşayan çok çeşitli mikroorganizmalar – yaklaşık 40 trilyon hücre – tarafından kolonize edilir. Mikrobiyomun insan sağlığına ve hastalığa olan derin katkıları günümüzde daha iyi anlaşılmıştır. Örneğin, araştırmacılar bu mikroorganizmaların bazılarının kanser gelişimi, ilerlemesi ve tedaviye yanıt üzerinde koruyucu veya zararlı etkiler gösterebileceğini bulmuşlardır.
- Yaşlanmış hücreler: Kanserin 14 Temel Özelliği hakkındaki bu yeni makale, yaşlanan hücrelerin tümör mikroçevresini besleyen araçlar olarak önemini de vurguladı. 2000 yılındaki makalede yazarlar, yaşlanmayı kanser ilaçları için bir engel olarak incelerken, bunun gerçek bir hücre değil de hücre parçacıkları yığını olma olasılığını düşünmemişlerdi. Yirmi yıldan fazla bir süre sonra, hücresel yaşlanmanın doku iç-dengesi ve kanserdeki rolü iyi bilinmektedir ve bununla ilişkili önemli morfolojik ve metabolik özellikler ortaya çıkarılmıştır. Araştırmalar ayrıca belirli bağlamlarda yaşlanan hücrelerin tümör gelişimini ve kanserleşmeyi nasıl teşvik edebildiğini de göstermiştir. Bu nedenle Hanahan, yaşlanan hücrelerin tümör mikroçevresinin önemli bileşenleri olarak dahil edilmesi gerektiğini öne sürmektedir.
Son sözlerinde Hanahan, bazı ayırt edici özelliklerin artık iyi bir şekilde doğrulanmış olmasına rağmen, ortaya çıkan ayırt edici özellikler olarak eklenen en yeni özelliklerin, kanser araştırma topluluğu içinde tartışmayı teşvik etmek ve kanser biyolojisi anlayışımızı iyileştirmeye devam edecek yeni araştırmalara ilham vermek adına “deney balonları” olarak hizmet etmesini amaçlamaktadır.
Önümüzdeki on yılda yeni nice keşiflere…
Douglas Hanahan; Hallmarks of Cancer: New Dimensions. Cancer Discov 1 January 2022; 12 (1): 31–46.






