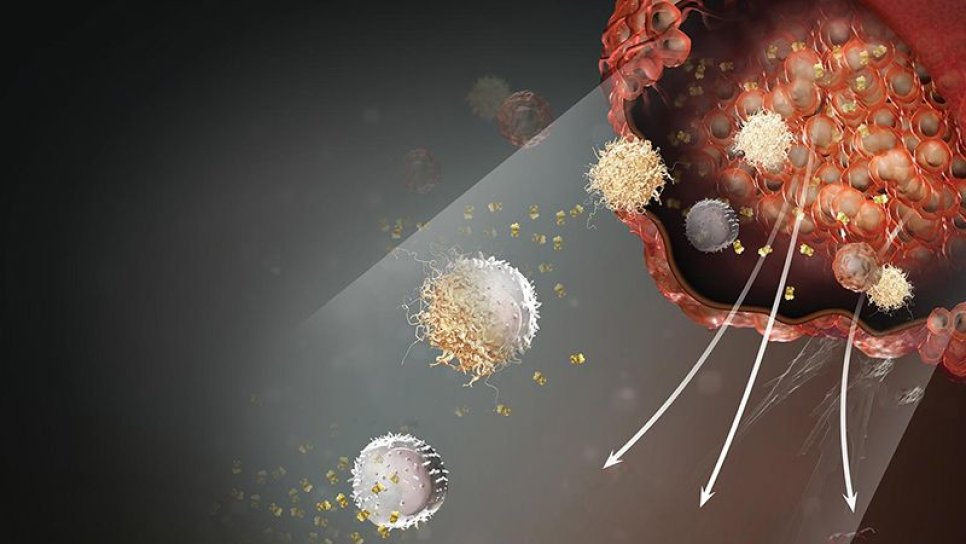
Yeni Bir Kanser İmmünoterapisi Geliyor: Makrofaj Kontrol Noktalarını Baskılamak
Tümör ilişkili makrofajları, kontrol noktaları olan CD47 üzerinden aktive etmek, yeni ve etkili bir kanser immünoterapi tedavisi olarak karşımıza çıkmaktadır.
Tümör mikroçevresi, kanser hücresinin çoğalmasını, yayılmasını ve ilaçlara direnç geliştirmesinde önemli rol oynamaktadır. Tümör mikroçevresinde bağışıklık sistemini baskılayan hücreler ve tümörün kendi yararına kullanmaya başladığı bağışıklık sistemi hücreleri bulunur. Makrofajlar tümör mikroçevresinde bulunan önemli hücrelerden biridir. Makrofajların normal şartlarda görevi bakteriler gibi patojen mikroorganizmalara ve tümörlere karşı ilk savunma sistemini oluşturmaktadır. Bu sistemi fagositoz ve hücre dışı birtakım mekanizmalarla yapar.
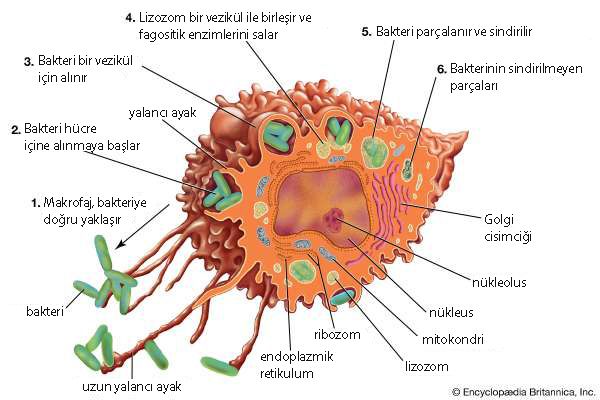
Aşağıdaki şekilde, bir makrofaj hücresinin (büyük turuncu hücre), bakterilere (küçük yeşil hücreler) saldırması ve yok etmesi resmedilmiştir.
İlgili Konu:
Ancak tümör ilerlemeye başladığında, bağışıklık sistemini ve bu sistemin elemanlarından biri olan makrofajları kendi yararına kullanır. Bu durumda makrofajlar, tümör ilişkili makrofaja dönüşür.
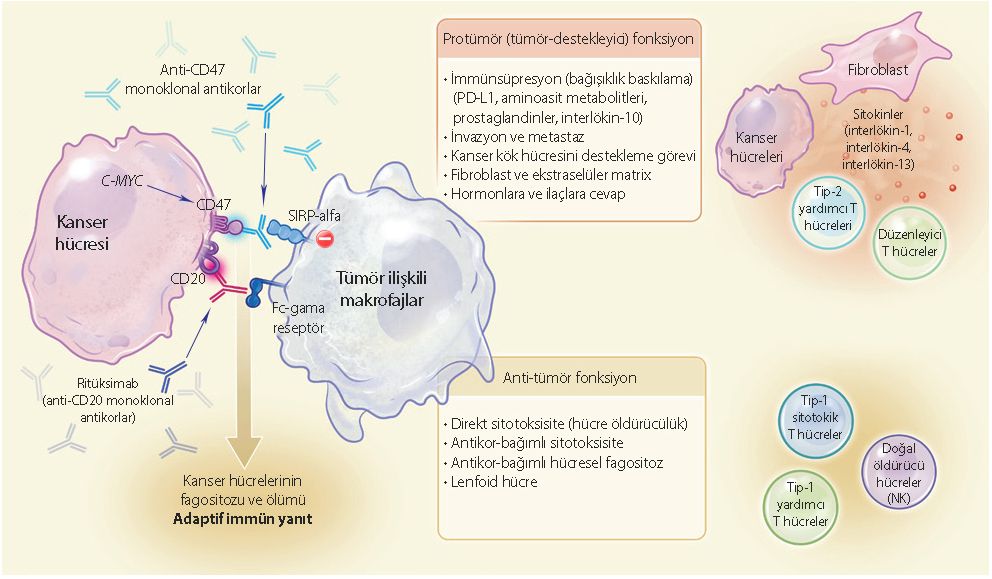
Yukarıdaki şekilde, makrofajların tümör destekleyici ve anti-tümör özellikleri gösterilmektedir. Yani bağışıklık sisteminin önemli elemanlarından biri olan makrofajlar, yerine göre tümör destekleyici, yerine göre de tümör karşıtı rol alabilmektedir.
Makrofajlar uygulanan kanser tedavilerine ve aktivasyon durumlarına göre anti-tümör (kansere karşı) ya da pro-tümör (kanseri destekleyici) özellik taşır. Tümör ilerlemeye başladığında, tümör ilişkili makrofajlar bağışıklık sistemini baskılama, metastaz ve invazyona (dokulara yayılma) yardımcı olma, kanser kök hücreleri destekleme, fibroblast ve ekstrasellülar matriksi (hücreler arası ortamlar) tümör destekleyici hale getirme gibi fonksiyonları gerçekleştirirler. Peki tümör ilişkili makrofajlar nasıl meydana gelir?
Kanser hücrelerinde, C-MYC adlı onkogenin aktivitesi oldukça fazladır ve bu gen, kanser hücrelerinin agresif biçimde çoğalmasını sağlar. C-MYC geni aynı zamanda CD47 geninin çalışmasını artırır. CD47 geni de CD47 adlı hücre yüzey reseptörünü üretir. Kanser hücrelerindeki CD47, makrofajların üzerindeki SIRPA proteinine bağlanır. Bu durumda, makrofaj kanser hücresini dost olarak görür ve saldırmaz. İşte bu yüzden CD47, makrofajların kontrol noktası olarak adlandırılmaktadır.
Bu bağlanmayı engellemek amacıyla CD47’yi hedef alan monoklonal antikorlar geliştirilmiştir. Anti-CD47 ve şu an bazı lösemi ve lenfomaların tedavisinde kullanımda olan anti-CD20 ile yeni kanser tedavi stratejisi oluşturulmaya çalışılmaktadır.
Bu amaçla gerçekleştirilen bir faz-1b klinik araştırmada, Hu5F9-G4 (anti-CD47) ve rituksimabın (anti CD20) etkinliği, standart tedavilere dirençli büyük B hücre lenfoma ve folikuler lenfoma hastalarında incelendi. Çalışmanın sonucunda tedaviye tam yanıt oranı, büyük B hücreli lenfomada yüzde 33, folikular lenfomada yüzde 43 bulundu. Beklendiği üzere anti-CD47 tedavisi anemi gibi yönetilebilir bir yan etkiye sebep olmaktadır.
Bu tedavide sağlanan başarı makrofajların direkt toksisite özelliğinin aktivasyonuyla ilgillidir (uygun şekilde aktifleşen makrofajlar, kanser hücreleri için direkt toksik/zararlı etkiye sahiptir).
Tümör hücresi genetik instabilitesi (tümör antijen yoğunluğunun yüksek olması), güncel T hücre hedefli kontrol noktası inhibitörü immünoterapisindeki başarıyı belirleyen önemli bir faktörken, makrofaj kontrol noktası blokaj tedavisi tümör antijenlerine bağımlı değildir.
Makrofaj blokaj tedavilerinin, T hücre blokaj tedavileri ile beraber kulanımı hem birincil hem de adaptif bağışıklık sistemi aktivasyonunu sağlayarak etkili bir kanser tedavisi sunabilir. Makrofaj blokaj tedavilerinde en önemli zorluk, hangi hastanın bu yeni immünoterapi tedavisine cevap vereceğini tanımlamaktır. İlginç bir şekilde, tümörün makrofajlarla yoğun bir şekilde infiltre (istila) edilmesi, kötü prognoz (hastalık gidişatı) ile ilişkilendirilmiştir.
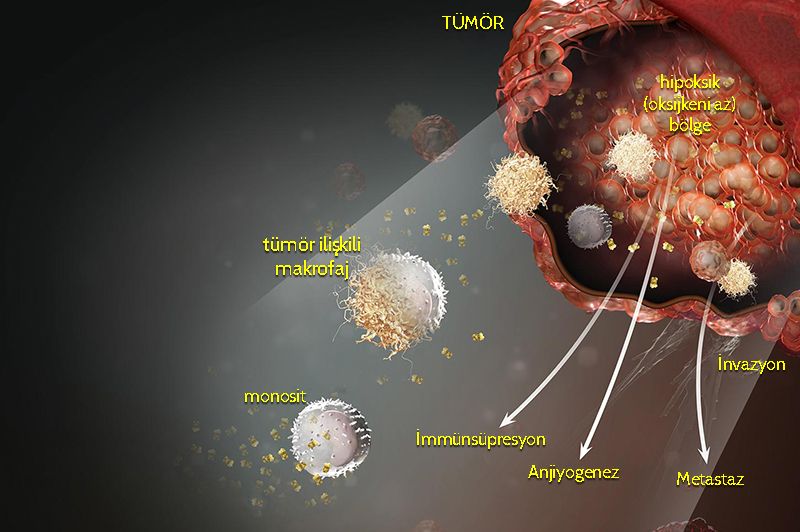
Aşağıdaki şekilde, monositlerin, tümör ilişkili makrofajlara dönüşümü ve daha sonra tümör mikroçevresine giden bu hücrelerin, tümörü hangi yollarla (invazyon, metastaz, anjiyogenez, immünsupresyon) desteklediği görülebilir.
Alberto Mantovani, M.D., and Dan L. Longo, M.D.
Macrophage Checkpoint Blockade in Cancer — Back to the Future.
NEJM, 1 November 2018






