Mide kanseri başlangıç tedavisinde ilk kez bir immünoterapi FDA onayı aldı
İlerlemiş veya metastatik mide, gastroözofageal bileşke ve özofagus adenokarsinomu için floropirimidin ve platin içeren kemoterapi ile kombinasyon halinde nivolumab (Opdivo) adlı immünoterapi 16 Nisan 2021'de FDA (ABD Gıda ve İlaç İdaresi) onayı aldı. Bu, mide kanserinin birinci basamak tedavisi için FDA onaylı ilk immünoterapidir.
Bu onay, ilerlemiş veya metastatik mide kanserli hastaların birinci basamak tedavisi için bir hayatta kalma faydası gösteren on yıldan fazla bir süredir ilk tedavidir.
Türkiye'de her yıl yaklaşık 13 bin yeni mide kanseri teşhisi konulmaktadır. Halihazırda mevcut olan tedavi ile genel sağkalım genellikle zayıftır; ameliyata rağmen tam şifa oranı çok düşüktür ve tüm evrelerin dahil edildiği bir istatistik için 5 yıllık genel sağkalım oranı % 32'dir.
Opdivo, bağışıklık sisteminin bir elemanı olan T hücrelerin fonksiyonunu artırarak tümör büyümesini inhibe eden monoklonal antikor sınıfından yeni nesil bir immünoterapidir.
CHECKMATE-649 çalışması ile gelen FDA onayı
Opdivonun bu kanserlerde etkinliği, önceden tedavi edilmemiş ilerlemiş veya metastatik mide, gastroözofageal bileşke ve özofagus adenokarsinomu olan 1.581 hastanın katıldığı randomize, çok merkezli, açık etiketli bir çalışmada değerlendirilmiştir.
Hastalar kemoterapi artı immünoterapi (789 hasta) veya tek başına kemoterapi (792 hasta) aldı; çalışma ilaçları şu şekilde uygulandı:
- 2 haftada bir mFOLFOX6 (florourasil, lökovorin ve oksaliplatin) artı 240 mg nivolumab (Opdivo) ya da 2 haftada bir mFOLFOX6.
- 3 haftada bir CapeOX (kapesitabin ve oksaliplatin) artı 360 mg nivolumab ya da 3 haftada bir CapeOX.
Sonuçlar
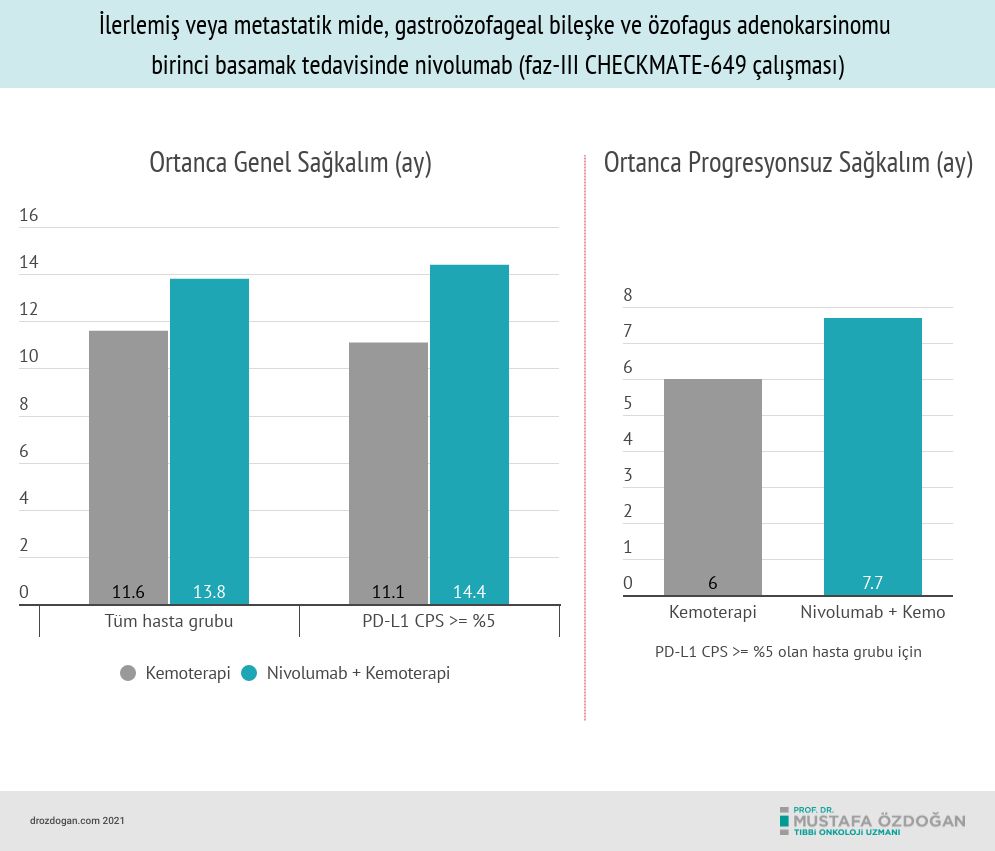
- Kemoterapi ile kombinasyon halinde Opdivo alan 789 hastanın ortanca genel sağkalım süresi, tek başına kemoterapi alan 792 hastadan daha uzun idi. Ortanca genel sağkalım, Opdivo artı kemoterapi alan hastalarda 13,8 ay iken, tek başına kemoterapi alan hastalarda 11,6 aydı.
- Bu fark PD-L1 kombine pozitif skoru (CPS) ≥5 olan hastalarda daha fazla idi: 14.4 aya karşı 11.1 ay.
- Ortanca progresyonsuz sağkalım (PFS), nivolumab artı kemoterapi kolunda 7.7 ay iken tek başına kemoterapi kolunda 6 idi (HR 0.68;% 95 CI: 0.58, 0.79; p <0.0001).
Yan etkiler
Opdivo'nun kemoterapi ile birlikte en yaygın yan etkileri arasında periferik nöropati (beyin ve omurilik dışındaki sinirlere zarar), bulantı, yorgunluk, ishal, kusma, iştah azalması, karın ağrısı, kabızlık ve kas-iskelet ağrısı bulunur. Opdivo, akciğerler (pnömoni), kolon (kolit), karaciğer (hepatit), endokrin bezleri (endokrinopatiler) ve böbrekler (nefrit) gibi sağlıklı organların iltihaplanması dahil, bağışıklık aracılı yan etkiler olarak bilinen ciddi durumlara neden olabilir. Hastalar, bağışıklık sistemi sorunları, akciğer veya solunum sorunları, karaciğer sorunları, organ nakli olmuşlarsa veya hamile iseler veya tedaviye başlamadan önce hamile kalmayı planlıyorlarsa bunu sağlık uzmanlarına söylemelidir.
Önerilen nivolumab dozajları şunlardır:
- Her 3 haftada bir CapeOX kemoterapisi ile kombinasyon halinde her 3 haftada bir 360 mg nivolumab.
- 2 haftada bir mFOLFOX6 kemoterapisi ile kombinasyon halinde 2 haftada bir 240 mg nivolumab.
FDA approves nivolumab in combination with chemotherapy for metastatic gastric cancer and esophageal adenocarcinoma. fda.gov 16 April 21