Glioblastom (GBM) ile ilişkili kritik genler: IDH-1/2
Yapılan araştırmalar glioblastom (GBM) oluşumu ve ilerleme sürecinde pek çok genetik faktörün etkili olduğunu göstermiştir. Bu genlerden bir tanesi de Izositrat DeHidrogenaz (IDH) genidir. Bu yazımızda kısaca IDH geninin işlevlerinden başlanarak GBM tedavisindeki yerine değinilecektir.
IDH 1/2 nedir?
IDH 1 ve 2, IDH 1 ve 2 genleri tarafından kodlanan metabolik enzimlerdir. Bu enzimler hücre içinde pek çok farklı işleve sahiptir ve bunların en önemlilerinden birisi enerji üretiminde rol alan Krebs döngüsü'ndeki yeridir. Bu döngü, canlı hücrelerin besinlerden enerji elde etmesini sağlayan önemli bir kimyasal süreçtir.
Yapılan genetik çalışmalar sonucunda IDH1/2 genlerinin düşük dereceli gliomaların %70-80’inde ve ikincil glioblastomların da büyük bir kısmında gözlendiği tespit edilmiştir. Bu veriler, GBM sınıflandırmasına yeni bir boyut kazandırmış ve IDH-mutasyonlu GBM (genellikle ikincil GBM’leri temsil eder) ve IDH-mutasyonsuz GBM (birincil GBM’leri içermektedir) olmak üzere iki sınıfa ayırır.
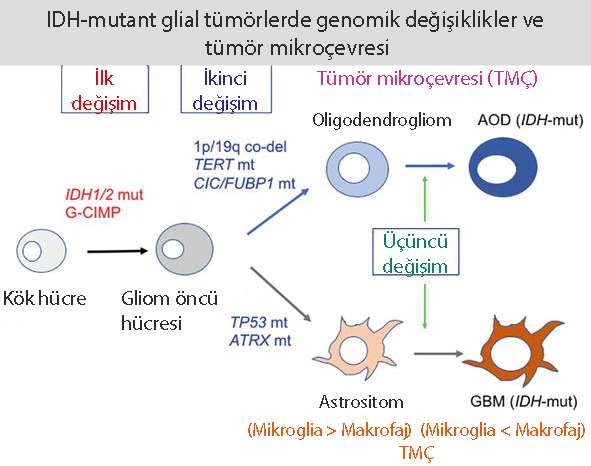
IDH 1/2 mutasyonlarının hücre düzeyinde etkileri nelerdir?
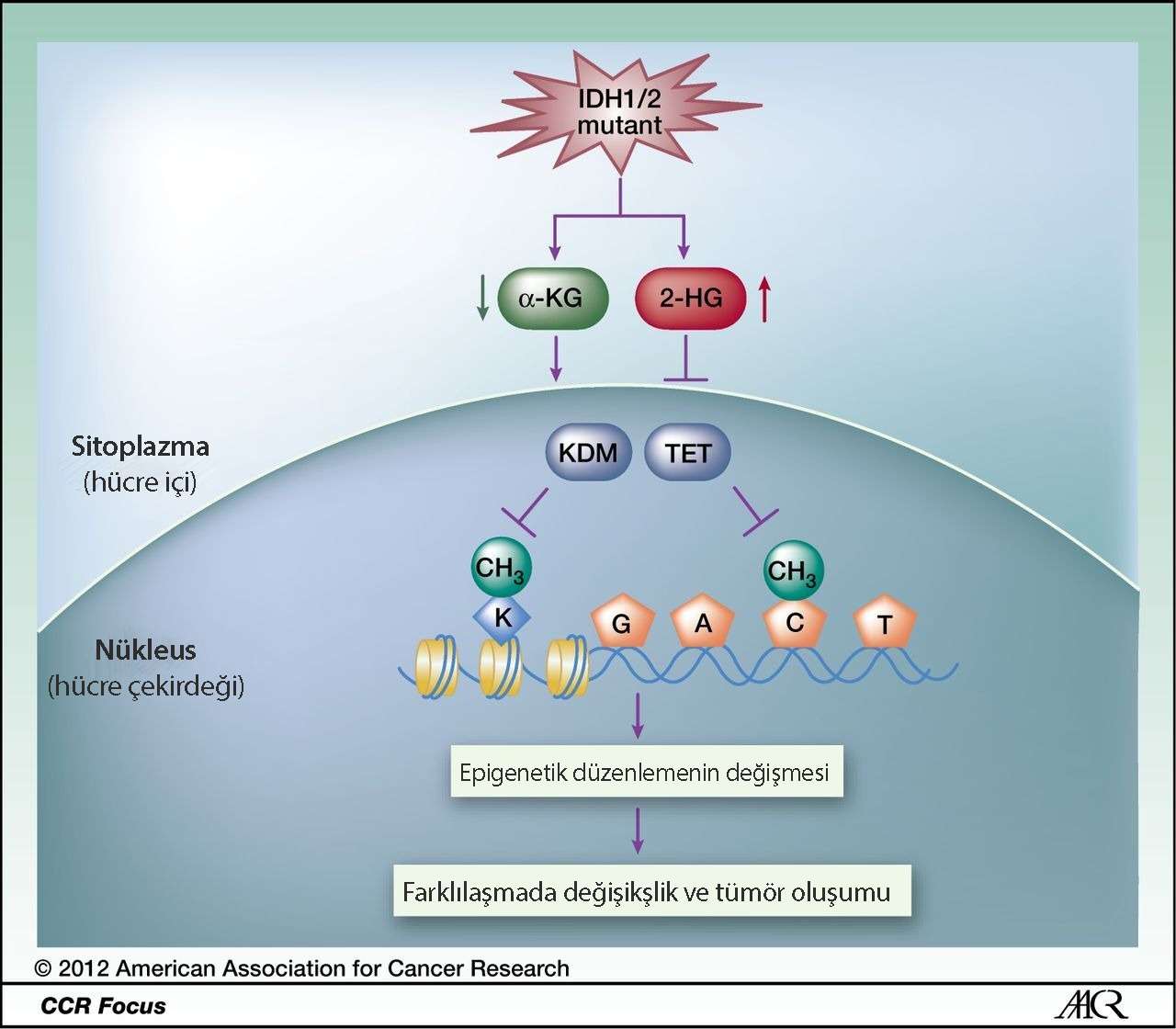
Alfa ketoglutarat (α-KG) enerji üretimi sırasında Krebs döngüsü içinde üretilen bir bileşiktir. Mutasyon sonucu fonksiyonu değişen IDH1/2 enzimleri KG’nin bir başka ara bileşik olan alfa hidroksiglutarik asite (2-HG) dönüşmesine neden olur. Vücutta 2-HG birikmesi hücresel döngüler için önemli olan enzimlerin fonksiyonlarını bozarak hücresel metabolizmayı ve epigenetik düzenlemeleri değiştirir, DNA onarım mekanizmasını bloke ederek tümör oluşumuna katkıda bulunur. Ayrıca histon ve DNA’dan metil gruplarının uzaklaştırılmasını sağlayan demetilaz enzimlerinin etkisini durdurmakta ve hücre farklılaşma döngüsünü bozmaktadır. Bunun yanında tümör oluşumuna katkıda bulunan yeni damar oluşumunu hızlandırmakta ve hücrelerin az oksijenli ortamda yaşamalarını destekleyecek genleri aktif hale getirmektedir.
IDH 1/2 mutasyonu saptanan tümörler nelerdir?
IDH1 ve IDH2 mutasyonları pek çok tümörde bulunmakla birlikte özellikle, 2. ve 3. derece astrositomlar, oligodendrogliomlar, oligoastrositomlar, ikincil gliblastomalar, kondrosarkomlar, anjiyoimmünoblastik t-hücreli lenfomalar, intrahepatik kolanjiyokarsinomlar, akut miyeloid lösemiler, cilt kanserleri, miyelodisplastik sendromlar, miyeloproliferatif neoplazmlar, kolon ve akciğer kanserlerinde karşımıza çıkmaktadır.
- Safra yolu kanserinde IDH hedefli tedaviler fark yarattı
- İleri evre over (yumurtalık) kanseri için IDH 1 hedefinin önemi keşfedildi
IDH inhibitörlerinden ABD Gıda ve İlaç Dairesi (FDA) onayı alan ilaçlar nelerdir?
Akut miyeloid lösemi için onaylanmış IDH1 bloke edici ajan ivosidenib (Tibsovo) ve IDH2 bloke edici enasidenib kullanılmaktadır. İki ilacın da temel mekanizması mutasyon sonucunda meydana gelen 2-HG artışını hedef almak ve bu etkiyi ortadan kaldırarak normal düzeylere getirmektir. Yapılan araştırmalar sonucunda Tibsovo kullanımı sonrasında hastalar da en sık gözlenen yan etkiler yorgunluk, eklem ağrıları, düzensiz kalp atışı, ishal, nefes darlığı, öksürük ve kabızlıktır. Bunun yanında enasidenib kullanımı sonrasında ortaya çıkan yan etkiler ise bulantı, kusma, ishal ve iştah azalmasıdır.
GBM'de IDH inhibitörleri test edildi mi? Sonuçları nelerdir?
IDH mutasyonlarının ikincil glioblastomlarda yaygın olarak gözlenmesi sonucu tümör oluşumunu tetiklediği düşünülmektedir. Bu nedenle GBM hastalarında uygulanmak üzere IDH baskılayıcı ajanlar çalışılmaya başlanmıştır.
Japonya’da yapılan DS-1001b isimli kan-beyin bariyerini geçerek hedef bölgeye ulaşabilen IDH1 baskılayıcı ajan için faz 1 klinik çalışması yapılmıştır. Tedavi sonrasında, 9 hastadan 2’sinin iyileşmeye yönelik küçük tepkiler verdiği, kalan hasta grubunda ise stabil bir ilerleme olduğu gözlenmiştir. Ayrıca yapılan bir başka çalışmada da 29 hastanın bir tanesinde tam tepki gözlenirken diğerlerinde yanıt alınamamıştır.
New York merkezli yapılan bir diğer çalışmada ise beyin tümörü ameliyatı mümkün olan tümör kitlesi çıkarıldıktan sonra IDH baskılayıcı ajanları kullanılan hastalarda 2-HG seviyesinin daha düşük olduğu gözlenmiştir. Aynı ekip, düşük 2-HG seviyesinin, kemoterapi ve radyasyon tedavisi alan hastalarda yaşam kalitesini arttığını belirtmiştir.
Yapılan diğer araştırmalar, IDH’de mutasyon bulunması hastalar için daha iyi bir prognoz (hastalığın sonucunu tahmin) sağlamakta bu nedenle enzimin baskılayıcı ajanlarla susturulması tümörün daha agresif olmasına neden olabileceğine değinilmiştir. Bu nedenle yeni bir baskılayıcı ajan olarak DNA tamir mekanizmasında görev alan Poli (ADP-Riboz) Polimeraz (PARP) proteini hedef alınmıştır. IDH enzimlerinde meydana gelen mutasyonlar gliom hücrelerinin PARP baskılayıcı ajana olan duyarlılığını arttırdığı gözlemlenmiştir. Kan-beyin bariyeri PARP baskılayıcı ajanların hedef bölgeye ulaşmasında engel oluşturduğu için GBM ile ilgili çalışmalar diğer kanserler ile yapılan çalışmalar kadar hızlı ilerlememektedir. Ancak yapılan deneylerde PARP baskılayıcı ajanların kullanımı GBM hastalarını radyasyon tedavisine duyarlı hale getirmektedir.
Molenaar, R.J., Maciejewski, J.P., Wilmink, J.W. et al.
Wild-type and mutated IDH1/2 enzymes and therapy responses. Oncogene 37, 1949–1960 (2018).
Kaminska, B., Czapski, B., Guzik, R., Król, S. K., & Gielniewski, B.
Consequences of IDH1/2 Mutations in Gliomas and an Assessment of Inhibitors Targeting Mutated IDH Proteins.
Molecules 2019 (Basel, Switzerland)
Waitkus MS, Diplas BH, Yan H.
Biological role and therapeutic potential of IDH mutations in cancer.
Cancer Cell 2018.
IDH inhibitors target common glioma mutation.
Cancer Discov. 2018.