Beyin tümörü glioblastoma multiforme (GBM) tedavisinde gelinen son nokta
Gliblastoma multiforme, beynin önemli yardımcı hücreleri olan glial hücrelerden türeyen yetişkinlerde en sık gözlenen primer (birincil) beyin tümörüdür; GBM, GBM-IV ve 4. derece beyin tümör adları ile de bilinmektedir. Hızlı ilerlemesi ve kesin bir tedavisinin olmayışı yaşam süresinin kısalmasına neden olsa da her yeni günde yapılan çalışmalar bizlere yeni tedavi yöntemleri sunmakta ve yaşam kalitemizi arttırmamıza yardımcı olmaktadır. Bu yazımızda sizlere hastalığın teşhisinden tedavi sonrası takibine kadar geçilen yollardan ve yeni tedavi yaklaşımlarından bahsedilecektir.
GBM belirtileri nedir, nasıl tanı konur?
Glioblastom hastaları günler ile haftalar arasında değişen yavaş ilerleyici nörolojik belirtilerle sağlık kurumlarına başvurmaktadırlar. Belirtiler tümörün yerleşim yerine ve büyüklüğüne bağlı olarak değişmektedir. En sık görülen belirtiler; baş ağrısı, epilepsi nöbeti, hafıza kaybı, bilişsel ve kişilik değişiklikleridir. Manyetik rezonans (MR) görüntüleme, beyin tümörlerinin tanısı, evrelemesi ve tedavi planlamasından en sık tercih edilen radyolojik yöntemdir. Görüntüleme ve teşhisin ardından tedavinin ilk aşaması olarak cerrahi müdahale yapılmaktadır. Sağlıklı beyin dokularına minimum hasar verecek şekilde mümkün olduğunca kitle temizlenmeye çalışılır. Cerrahi müdahale sırasında alınacak parçaların patolojik incelemesi başlanacak tedavinin karar verilmesi noktasında oldukça önemlidir.
GBM'de ameliyatla tümörü tam çıkarma, neden çoğu zaman mümkün değildir?
GBM, sinir hücrelerini destekleyen glial hücrelerin kanseridir ve bu nedenle glioblastom türünde beyin tümörleri, yıldız şeklinde ışınımsal büyür. Glioblastom tümörlerinin bu düzensiz / yıldızsı yapısı, normal beyin dokusu içine saçaklı bir şekilde girmesine neden olur. Tümörü ameliyatla tamamen çıkarmak büyük bir beyin dokusu kaybına yol açacağı için tümör, "olabildiğince" çıkarılır.
Cerrahi müdahalenin ardından radyoterapi tedavisine başlanılır. Bu terapide amaç X-ray veya protonlar gibi yüksek enerjili ışınları ile kalan tümör hücrelerini öldürmek ve yayılmalarını önlemektir. Radyoterapiyi takiben kemoterapi tedavi süreci başlar. Temozolomid, beyin tümöründe en sık tercih edilen kemoterapi ilacıdır ve hap şeklinde oral olarak alınmaktadır. Yapılan çalışmalarda temozolomidin radyasyon tedavisi ile aynı anda verilmesinin yaşam süresini uzattığı gözlenmiştir. Ancak burada önemli olan, verilen tedavinin dozuna bağlı olarak düzenli aralıklarla kan testlerinin yapılması ve trombosit (kan pulcuğu), lökosit (akyuvar) gibi kan hücre değerlerinin takip edilmesidir. Bazı vakalarda, kemoterapötik ajanları içeren ve tümör dokusunda ilaç salınımı yapan kapsüller cerrahi müdahaleler sırasında implante edilebilir (Carmustine polymer wafers- Gliadel). Ancak yeni teşhis konulan hastalarda radyasyon tedavisi ile birlikte kullanılan kapsüllerin güvenilirliği tam olarak belirlenememiştir.
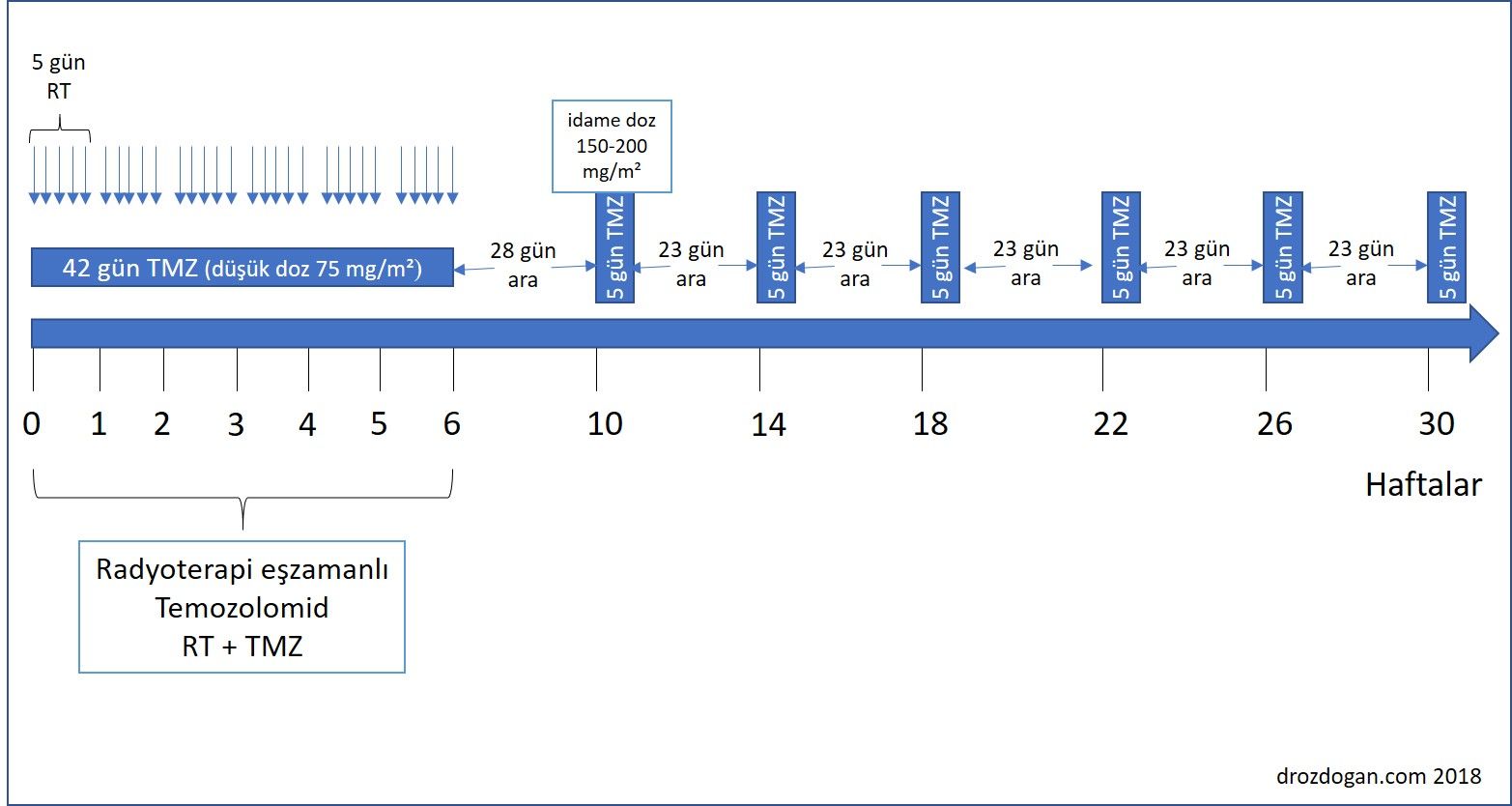
- İlgili konu: Temozolomid nedir ve nasıl kullanılır? (detaylı)
Güncel çalışmaların bize sağladığı bir diğer terapötik yaklaşım immünoterapidir. Farklı kanser türlerinde onay almış bu yeni kanser tedavi yöntemi glioblastoma için de denenmektedir, fakat henüz bu kanser türünde FDA onayı almamıştır. Bağışıklık sistemimizin önemli hücrelerinden olan dendritik hücreler ile hazırlanan kanser aşılarının (DCVax-L, Northwest Biotherapeutics) ortalama yaşam süresini faz-2 çalışmalarında uzattığı belirlenmiştir. Kanser hücrelerinin antijenlerinden yapılan aşılar bir diğer tedavi çeşididir. Burada amaç, tümör hücrelerinin yüzey belirteçlerinden ya da tümöründen kendisinden yapılan aşıların hastanın bağışıklık sistemini harekete geçirmesidir. En çok çalışılan tümör spesifik antijen olarak EGFRvIII ile yapılan aşı denemelerinin faz 1 ve 2 sonuçları umut vericidir.
Bir diğer gelecek vadeden immünoterapi yöntemi CAR-T canlı hücre (kimerik antijen reseptör- T hücresi) tedavisidir. Laboratuvar ortamında T hücrelerine eklenen özel reseptörler kanser hücrelerini spesifik olarak hedef alacak şekilde tasarlanmıştır. Klinik öncesi (pre-klinik) modeller üzerinde yapılan çalışmalarda CAR-T hücrelerinin tümör hücrelerini başarılı olarak hedef aldıkları gözlenmiştir.
Biyoteknolojik bir buluş olan Optune, glioblastoma tedavisi için onay almış bir diğer yöntemdir. Burada amaç, alternatif elektrik akımı ile sağlıklı beyin dokularını etkilemeden kanser hücrelerinin çoğalmasını durdurmaktır. Etkisini arttırması amacıyla temozolomid tedavisi ile birlikte yapılan çalışmalarda, sağkalımda gözlemlenen artış oldukça önemli bir gelişmedir.
Yukarıda belirtilen tedavi yöntemlerinin yanı sıra devam etmekte olan pek çok klinik çalışma vardır. Burada en önemli sorun çalışmaların faz 1 aşamasından faz 2’ye veya faz 2 aşamasından faz 3’e geçememesidir. Yapılan çalışmalar bu sorunun sebebi, glioblastom tümörlerinin oldukça heterojen - biyolojik ve genetik olarak çok çeşitli - bir hastalık grubu olması olarak gösterilmektedir. Bu noktada günümüzün en popüler araştırma konularından olan tümörün genetik olarak haritalandırması, gelecekte tasarlanacak hedefe yönelik kanser tedavileri için büyük bir rol oynamaktadır.
GBM'de her tedavi planı kişiye özel yapılmaktadır. Teşhisin ilk aşamasından itibaren dikkatli inceleme sonucu en doğru tedavi yöntemi ve dozu belirlenmelidir. Ayrıca onkolojik rehabilitasyon, GBM hastalarında tanıdan itibaren düşünülmelidir. Ancak yazının başında da belirtildiği gibi süreç burada bitmemektedir. Tedavi sonrası yapılacak düzenli kontroller de tedavi süreci kadar önemlidir.
Glioblastom, genel olarak sağkalım oranının düşük olması ile anılsa da, her yıl yeni ve umut verici çalışmalarla karşılaşmaktayız. Bu konuda yapılan çalışmaları takip edecek ve sizleri bilgilendirmeye devam edeceğiz.
*
İleri okuma: Temozolomidin etki ve direnç mekanizmaları
Temozolomid, DNA alkilleyici bir ajandır ve çift zincirli DNA hasarına sebep olarak tümör hücrelerinin ölmesine neden olmaktadır. Bu noktada, hastanın MGMT (O-6-methylguanine-DNA methyltransferase) adı verilen DNA onarıcı enzim geninin metil grubu içerip içermediği tedavi sonucunu etkilemektedir. MGMT geninde metil grubunun olması temozolomid tedavisinin sağkalım oranını arttırdığı yapılan çalışmalar ile kanıtlanmıştır. Temozolomide tedavisi gören hastaların tümör mikroçevresi (düşük oksijen konsantrasyonu, hücreler arası bağlantı molekülleri ve glioma kök hücreleri), DNA tamir mekanizması , mikro RNA, epigenetik değişiklikler ve hücre ölümleri (apoptoz) tedaviye direnç oluşturmakta ve sonucu etkilemektedir.