
Geleceğin kanser tedavileri için en önemli kilometre taşı: MUTASYON KATALOĞU
Kanserin tüm genom analizi veya tüm genomların pan-kanser analizi (Pan-Cancer Analysis of Whole Genomes, PCAWG) adlı projeye imza atan bilim insanları, 2600'den fazla kanser genomunun mutasyon olaylarını analiz ettikleri, daha önce benzeri görülmemiş veriler yayınladılar. 38 ana tümör tipinde genomun hem kodlayan hem de kodlamayan bölgelerindeki kanserle ilgili mutasyonların geniş ve kapsamlı bir portresini katalogladılar, birleştirdiler ve bu bilgileri, ilgili biyolojik yolları belirlemek için kullandılar.
Genom nedir?
Genom, DNA'daki tüm talimatların toplamıdır. Her bir hücremizin çekirdeğinde, biri anneden diğeri babadan gelen 2 DNA kopyası vardır. DNA'mız özel bir şekilde katlanarak / paketlenerek kromozomları oluşturur. Hücrelerimizin içinde 46 tane paketlenmiş DNA sarmallarının bulunduğu kromozomlar vardır (23’ü anneden ve 23’ü babadan gelen).
Tüm genomların pan-kanser analizi projesinin özeti:
- Her kanser genomunda yaklaşık beş sürücü mutasyonu tanımlanmıştır (% 5'inde sürücü mutasyonu yoktu).
- Sürücü mutasyonlarının çoğunun genomun kodlama bölgesinde olduğu bulunmuştur.
- Bir "moleküler saat", kanserin evriminde hangi mutasyonların erken gerçekleştiğini belirleyebilir.
- Genetik mutasyon paternleri kanser tipinin belirlenmesine yardımcı olabilir (bu, primeri / kaynağı bilinmeyen bir kanserin tanımlanması için doktorlara yardımcı olabilir).
37 ülkeden 1300'den fazla bilim adamı ve doktor arasındaki iş birliğini içeren bu kollektif çaba, Nature ve bağlı dergilerinde aynı anda yayınlanan 23 bilimsel makaleyle sonuçlandı.

Tüm genomların pan-kanser analizi veri seti, dünya genelinde tüm kanser araştırmacılarının kullanımına açılmış durumda. Bu kanser verisinin geniş kullanılabilirliği ve kalitesi neredeyse kesinlikle bir biyolojik kavrayış ve metodolojik gelişmeler dalgası yaratacaktır.
Örneğin, araştırmacıların mutasyonların daha erken mi yoksa daha sonra mı meydana gelip gelmediğini analiz ettikleri moleküler saatler üzerindeki çalışma, sonunda kanserin erken teşhisinde veya kanserden korunma stratejilerinde yararlı olabilir.
Genel olarak, çalışmanın bulguları, kanser teşhis edilmeden yıllar önce sürücü mutasyonlarının erken teşhis ve biyobelirteç gelişimi için etkileri olabileceğini gösteriyor. Kanser oluşumunda kritik role sahip sürücü mutasyonlar, kanser teşhisi konulmadan yıllar önce ortaya çıkabilir, bu da erken teşhis için kullanılabilir.
Bununla birlikte, kanserin tüm genom analizi gibi çıkarımsal analizlerin, kanser hakkında daha derin bir anlayış sağlamasına rağmen, genellikle daha yüksek bir kompleksite derecesi ile ilişkili olduğunu da unutmamak lazım.
Tüm genomların pan-kanser analizi – Kodlayan ve kodlamayan DNA bölgeleri
Tüm genomların pan-kanser analizi (PCAWG) çalışmasından toplanan bilgiler ve bu yeni anlayış, klasik tüm ekzom sekanslamadan farklıdır.
Not: Ekzom, DNA'nın protein kodlayan ekzon isimli bölgelerinin toplamıdır ve DNA'nın sadece %1'ini oluşturur; bu, protein kodlayan 20 bin gene karşılık gelmektedir. Yani tüm ekzom analizi, DNA'nın sadece %2'sindeki mutasyonları analiz etmektedir. İntronlar ise DNA'nın protein kodlamayan bölgeleridir ve hatta yakın zamana kadar junk (çöp, önemsiz) DNA olarak adlandırılmaktaydı.
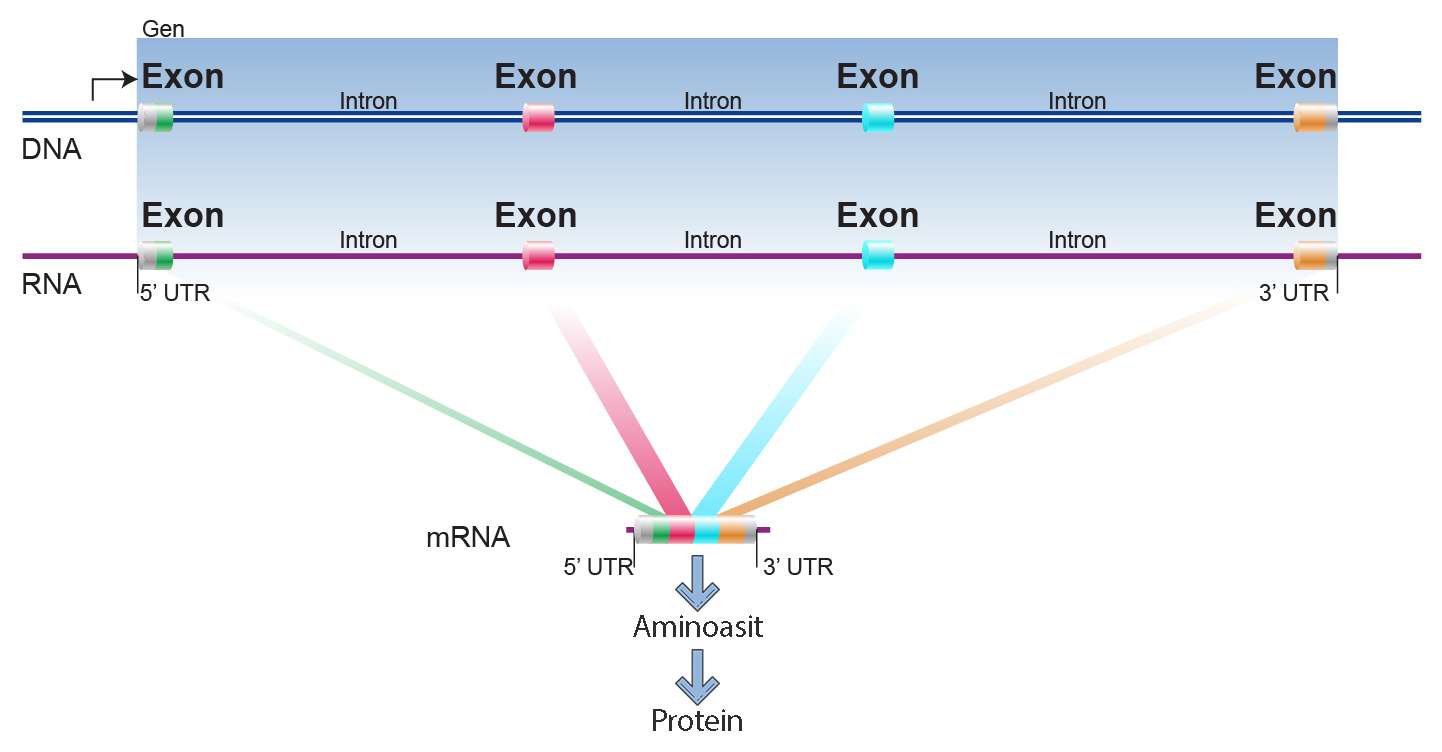
Şimdiye kadar kullanılan tüm hedefe yönelik akıllı kanser ilaçları, genomun sadece %1'ini temsil eden tüm ekzom sekanslamadan ortaya çıkan DNA dizilerine bakılarak geliştirilmişti. Şimdi ise kodlamayan bölgeler de dahil edilerek, kapsam %100'e çıkarılmış durumda.
Tüm genomların pan-kanser analizi projesinin hem ham hem işlenmiş hem de yorumlanmış verileri, diğer araştırmacılara gelecek yıllar için veri sağlamaya devam edecek şekilde PCAWG web sayfasında çevrimiçi olarak sunulmaktadır.
Pan-kanser analizi
Tüm-kanser analizi için, 2605 ana tümör ve 173 metastaz veya bölgesel nükse ait kanserli doku ve uyumlu normal dokuya ait tam genom sekans verisi kullanıldı. Veriler 3 ana grup mutasyon için analiz edildi: somatik tek nükleotid varyantları (SNV); küçük eklemeler ve silmeler (indeller); ve DNA'nın büyük kısımlarının yeniden düzenlenmesi olan kopya sayısı değişiklikleri ve yapısal varyantlar (SV).
Etkileyici bir şekilde kataloglama, > 43 milyon SNV, > 400.000 somatik çok çekirdekli varyantlar, > 2.4 milyon somatik indel, 290.000'e yakın somatik SV, > 19.000 somatik retrotranspozisyon olayı ve > 8000 de novo mitokondriyal DNA mutasyonu ortaya çıkardı. Analiz, tümör tiplerinin yanı sıra hastalar arasında somatik mutasyonların yükünde önemli bir heterojenlik rapor etmiştir.
Sürücü mutasyonlarının kataloglanması ve anlaşılması, son yirmi yıldır kanser araştırma topluluğunun önemli bir hedefi olmuştur ve sınırlı sayıda sürücü mutasyonu olmasına rağmen, bu sürücülerin binlerce veya onbinlerce kombinasyonu vardır.
Araştırmacılar, kanserlerin % 91'inin en az bir tanımlanabilir sürücü mutasyonuna sahip olduğunu buldular; tümör başına ise 4.6 sürücü mutasyon bulundu. Kanserlerin yaklaşık % 5'i için herhangi bir sürücü mutasyon bildirilmedi.
Tümör tiplerine göre incelendiğinde, sürücü SV'ler (yapısal varyantlar) meme ve yumurtalık adenokarsinomlarında daha yaygındı. Sürücü nokta mutasyonları kolorektal adenokarsinomlarda ve olgun B hücreli lenfomalarda önemli bir rol oynamıştır. Tümör baskılayıcı genlerle ilişkili birçok sürücü mutasyonu iki koldan inaktive edici idi: TP53'teki mutasyonların % 77'sinde her iki allel de mutasyona uğramıştı.
Kromofob renal hücreli karsinomlu ve pankreatik nöroendokrin kanserli hastalarda – ki bunlar kayda değer kromozomal anöploidi olan tümörlerdir – sürücü kanser mutasyonlar görülmedi. PCAWG araştırmacıları, "Tam kromozom kazanımlarının ve kayıplarının belirli kombinasyonları, daha hedefli sürücü mutasyonlarının yokluğunda, bir kanseri başlatmak için yeterli olabilir." şeklinde bu durumu ifade ettiler.
Aynı tanıya sahip iki hastanın tedavilere tamamen farklı cevap vermesinin altıdaki sebep, tümörlerin genetik farklılıklarıdır.
Bu durumun nedenleri tümörlerin genomunda yazılmıştır. Çarpıcı bulgu, bir kişinin kanser genomunun başka bir kişininkinden ne kadar farklı olduğudur - kansere neden olabilecek binlerce farklı mutasyon kombinasyonu ve 80'den fazla farklı süreç...
Tüm kanserlerin % 5 kadarı primeri bilinmeyen kanser (carcinoma of unknown origin) tanısı almaktadır. Mutasyon paternleri ve hangi genleri etkilediği, hastanın hangi kanser türüne sahip olabileceğini tanımlamaya yardımcı olabilir.
Kodlama yapmayan bölgelerdeki mutasyonlara yakın bakış
Kodlamayan somatik sürücülerin analizlerinde, NEAT1 ve MALAT1 uzun kodlamayan RNA'lar gibi önceden raporlanan kodlama yapmayan sürücüleri sorgulamakta, aynı zamanda yenilerini ortaya çıkarmaktadır.
PCAWG araştırmacıları, TERT promotöründe, daha yüksek TERT ekspresyonu ile ilişkili olan tek bölgeli sıcak noktalar buldu (promotör, genlerin transkripsiyonunu başlatan, DNA'parçasıdır).
TOB1'in mide ve meme kanserleri için etkileri vardı.
TP53 için promotör mutasyonlarının rapor edildiği durumlarda, kodlama bölgesinde ilave mutasyonlar yoktu, bu da ilk kez olarak kodlamayan mutasyonlardan TP53'ün güçlü bir inaktivasyonunu düşündürmektedir.
Araştırmacılar ayrıca AKR1C genlerini ve BRD4'ü içeren yeniden düzenlemeler gibi onkogenezi (kanserleşme) sürdürmeye aday yeni yapısal-varyant mutasyonlar bildirdiler.
Bununla birlikte, kodlama yapmayan sürücü mutasyonlar nadir olaylar olarak bulunmuştur. Araştırmacılara göre, daha büyük veri setleri ve teknolojik ilerlemeler, protein kodlayan sürücülerden çok daha düşük frekanslarda da olsa yeni kodlayıcı olmayan sürücüleri tanımlamaya devam edecek.
Moleküler saatler
Araştırmacılar ayrıca, kanserin evriminde mutasyonların erken mi yoksa geç mi meydana geldiğini de ele aldılar. Moleküler saatler kavramı, mutasyonların klonal (tüm kanser klonlarında meydana gelen) veya subklonal (kanser klonlarının bir kısmında meydana gelen) olup olmadığını ve subklonal olaylardan önce klonal olaylar olup olmadığının belirlenmesiyle ele alınmıştır.
2583 örnekte bulunan 47 milyon nokta mutasyonun % 22'sinin erken klonal olaylar; % 7'sinin ise geç klonal; % 53'ü tanımlanmamış klonal ve % 17'si ise tanımlanmamış subklonal olduğunu buldular. 453 kanser sürücüsü geninin bir panelinde % 29'u erken klonal, % 5'i geç klonal, % 56 tanımlanmamış klonal ve % 8' subklonal olay olan 5913 onkojenik nokta mutasyonu tanımladılar.
Sürücü mutasyonlar KRAS , TP53 ve PIK3CA ve kodlayıcı olmayan sürücü mutasyonlardan TERT, kanserlerin gelişiminde erken olayları kabul edildi. Araştırmacılar, mutasyonel imzanın tümörlerin % 40'ında zamanla değiştiğini belirtti.
Bir doktor bu bilgi servetini nasıl kullanmalı?
"Pan-Kanser Projesi, genomların nasıl toplanması ve analiz edilmesi gerektiği konusunda yol haritası sunuyor. Genomları analiz etmek ve bunları birleştirilmiş bir şekilde sunmak için yüksek kalitede standartlaştırılmış süreçler geliştirdik." diyor projenin başındaki isimlerden Dr. Lincoln D. Stein basın toplantısında. "Bu proje ile ekzom sekanslaması ile tanımlanan yolların aynısı bulundu, ayrıca bu yolları geliştirmek için daha birçok yol bulduk." diye ekliyor.
Ayrıca, belirli bir kanserde hangi sinyal / büyüme yollarının ve genlerin değiştirildiğini anlama yeteneğimizin artmasıyla, artık hastanın tümöründe meydana gelen değişiklikleri daha doğru bir şekilde görebileceğiz. Böylelikle daha hedefe yönelik tedaviler kullanabiliriz.
Bundan önce, sadece ekzom dizilişine baktığımızda, kliniğe gelen hastaların yaklaşık üçte birinde tümör genomu konusunda karanlıkta olacağız. Hassas onkoloji yapmaya devam edecek hiçbir bilgimiz olmayacaktı.
Bununla birlikte, bu çalışmaların önemli bir sınırlaması, hastaların tedavileriyle ilişkilendiren klinik verilerin olmamasıdır.
Devam eden ICGC ARGO projesi tam olarak bu eksiği tamamlamak için çalışıyor. PCAWG projesi yayınlarına ek olarak 100.000 kanser hastasının hem klinik hem genomik verilerini topluyorlar.
Genomik verileri klinik sonuçlarla ilişkilendiren yeterli veri topladıktan sonra, doktorun hastanın moleküler ve genomik bilgilerini kullanarak daha iyi tedavi seçenekleri belirlemesine yardımcı olacak makine öğrenme ve karar destek sistemleri oluşturulmaya başlanacak.
Bununla birlikte, kanser genom testi yakında herhangi bir kanser kliniğinde kullanılamayacak. Şu anda mevcut olan çoklu gen paneli testinden farklı olarak, tüm genom dizilemesinin laboratuvar süreçleri ve standardizasyonlarının genetik test merkezlerine aktarılması gerekecektir.
Ayrıca, bu yeni genetik test araçların çalıştırılması ve ortaya çıkan verilerin analiz edilmesiyle ilgili maliyetler de vardır. Şimdi oldukça pahalı, ama zamanla maliyetler düşecek. Bu teknoloji hemen yarın kullanıma girmeyecek, ancak birkaç yıl içinde daha kolay bir şekilde kullanılabilir olacak.
İlgili Konu:
- Yeni nesil dizileme (Next-Generation Sequencing, NGS) nedir? Onkolojide kullanımı
1. The ICGC/TCGA Pan-Cancer Analysis of Whole Genomes Consortium
Pan-cancer analysis of whole genomes
Nature, 05 February 2020
2. Milestone' Catalogue of Mutations in the Cancer Genome - Medscape - Feb 07, 2020.






