
PARP inhibitörleri – Over kanseri tedavisini değiştiren yeni bir ilaç sınıfı
Over kanseri – Önemi ve istatistikler
Gelişmiş ülkelerde, yaşam kaybına neden olan tüm jinekolojik (kadınlara özgü) kanserler arasında over (kadın yumurtalık) kanseri oldukça ciddi bir orana sahiptir. Dünya Sağlık Örgütü’ne (DSÖ) göre 2018 yılında dünya genelinde yaklaşık 295,000 yeni yumurtalık kanseri vakası tespit edilmiş ve 185,000 kişi yaşam kaybına gitmiştir. Yumurtalık kanserinin erken evrelerde teşhis edilmesi zor olduğu için, hastaların büyük bir çoğunluğu ileri evrelerde başvurmaktadır. Yapılan araştırmalara göre, tanı anında yumurtalık kanseri teşhisi alan kişilerin %59’unun metastatik evrede olduğu ve %21’lik kısmın ise lenf düğümlerine yayılım göstererek bölgesel ileri evre olduğu bilinmektedir. Metastatik epitelyal yumurtalık kanseri olan kişilerde 5 yıllık göreceli sağkalım oranı sadece %29,2’dir.
Yeni tanı alan ve ileri evre yumurtalık kanseri olan kişiler için ilk tedavi genellikle cerrahi müdahale ile başlamaktadır. Bu cerrahi müdahale, total histerektomi (rahmin alınması) ve görülen tüm tümörlerin ameliyatla çıkarılması olarak da bilinen sitoredüktif cerrahi müdahaleyi kapsamaktadır. Sitoredüktif cerrahide amaç, karın içinde yumurtalar, rahim, karın zarı ve lenf bezleri dahil olmak üzere mümkün olduğu kadar çok kanserli dokuyu ameliyatla çıkartmaktır. Cerrahi işlemleri platin bazlı kemoterapi ile birlikte vasküler endotelyal büyüme faktörü (VEGF) inhibitörünün kullanıldığı bevasizumab tedavisi izlemektedir. Ameliya sonrası uygulanan ana tedaviyi, yeni damar önleyici bevasizumab veya BRCA mutasyonu olan hastalarda poli ADP riboz polimeraz (PARP) inhibitörünün kullanıldığı idame tedavi izlemektedir (ana tedavi sonrası kanser tekrarı ihtimalini azaltıcı uygulama). Eğer kişi cerrahi müdahale için uygun değilse veya sitoredüktif cerrahi ile alınacak verim düşük ise, neoadjuvan (ameliyat öncesi küçültücü) tedaviler uygulanabilir.

Birinci basamak tedaviye iyi yanıt alınmasına rağmen, yumurtalık kanseri olan kişilerin büyük çoğunluğu tanı aldıktan 2 yıldan daha kısa bir süre sonra tekrarlamaktadır. Ancak birinci basamak tedavilerden sonra progresyonsuz (ilerlemesiz) sağkalımın uzun olması, kanserin tekrarlaması durumunda uygulanacak ikinci kemoterapilere verilecek yanıtları arttırmaktadır. Bu nedenle, hastaya en uygun tedavi seçeneğini bulmak ve standart protokolün dışında klinik yanıtı daha yüksek olan tedavi seçeneklerini belirlemek son derece önemlidir.

Genetik testlerin, tedavi seçeneklerinin belirlenmesindeki rolü
İleri evre yumurtalık kanseri olan kadınlar için pek çok tedavi seçeneği mevcut olsa da, seçilen tedavi yöntemi her hasta için uygun olmamaktadır. Bu nedenle, tedavi yöntemleri hastanın tümör özellikleri göz önünde bulundurularak seçilmelidir.
Genetik / moleküler testler artık over kanseri tedavi planı olmazsa olmazdır ve doğru tedavi yöntemini belirlemede ilk adımdır: Yumurtalık kanseri olan her kadın, tedaviden en iyi verimi alabilmek ve yumurtalık kanserine yatkınlık geni taşıyan gelecek nesillerde kanseri önlemek için mutlaka gen testi yaptırmalıdır.
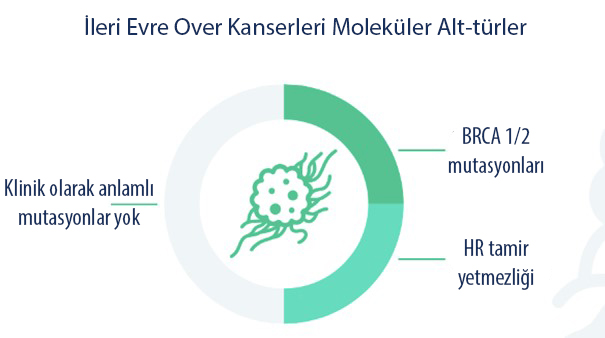
En yaygın görülen yumurtalık kanseri türü olan ileri evre seröz yumurtalık kanserinin yaklaşık %50’si germ hattı (kalıtsal) veya somatik mutasyon kaynaklı homolog rekombinasyon onarım eksikliğine sahiptir. Ve bu kişilerin PARP inhibitörlerinden fayda sağladığı bilinmektedir.
Yapılan çalışmalar sonucunda, BRCA geninin yumurtalık/fallop tüpü kanserlerinin gelişmesinde önemli bir rol oynadığı tespit edildi. Yumurtalık kanseri olan kadınların yaklaşık %10 ila %15’i germ hattı (kalıtsal) BRCA mutasyonuna sahipken, yaklaşık %7’si somatik (kalıtsal olmayan) BRCA gen mutasyonları barındırmaktadır. Bu mutasyonun dışında hastalar BRCA ile ilgisi olmayan birkaç başka mutasyon daha taşımaktadır. Yumurtalık kanserinde, BRCA1/2 mutasyonu taşıyan hastalar farklı klinik özellikler göstermekle birlikte tedaviye verdikleri yanıtlar da değişiklik göstermektedir.
BRCA geni, homolog rekombinasyon (HR) ile DNA tamirinde rol almaktadır. Bu nedenle BRCA genlerinde meydana gelen mutasyonlar, HR eksikliğine neden olmaktadır. İleri evre over kanseri olan hastalarda BRCA1/2 testinin yanında HR eksikliği ve diğer kalıtsal kanser genleri de test edilmeli.
Homolog rekombinasyon eksikliği (homologous recombination deficiency, HRD) nedir?
Homolog rekombinasyon eksikliği (HRD) durumu şu şekilde tanımlanmıştır: zararlı veya şüpheli zararlı bir BRCA mutasyonu veya son platin bazlı kemoterapiye yanıt verdikten altı aydan daha sonra hastalık ilerlemesi olan hastalarda genomik instabilite.
PARP inhibitörleri kanser tedavilerini nasıl değiştiriyor?
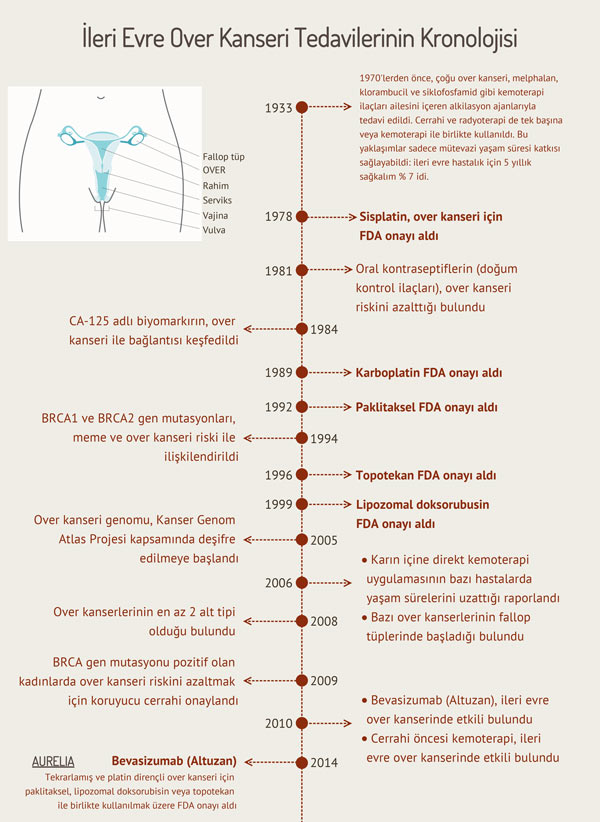
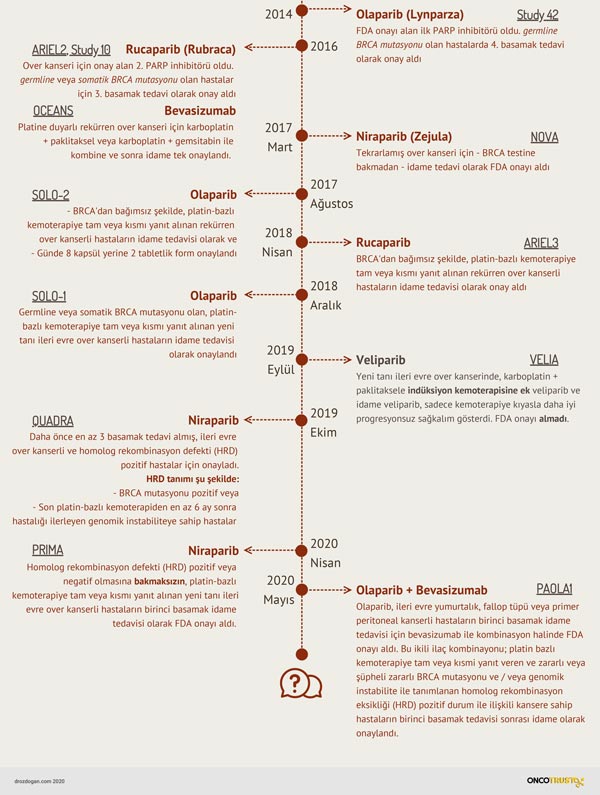
PARP inhibitörlerinin kullanıma başlanması ile yumurtalık kanseri olan birçok hasta için hastalığın seyri değişti. 2014 yılında Amerikan Gıda ve İlaç İdaresi (FDA), daha önce üç veya daha fazla basamak kemoterapi tedavisi almış, zararlı germ hattı BRCA mutasyonu olan ileri evre yumurtalık kanserinde kullanılmak üzere ilk PARP inhibitörü olan olaparib (Lynparza) için onay verdi. Günümüzde 3 PARP inhibitörü (olaparib, rucaparib, niraparib) yumurtalık kanserinde kullanılmak üzere FDA tarafından onaylanmıştır. Ayrıca yakın zamanda, bu inhibitörlerin BRCA1/2 mutasyonu pozitif olmasa bile, platin bazlı tedavi ile tam veya kısmi yanıtlı yumurtalık kanserinde birinci basamak idame tedavisi olarak kullanımına dair yeni bir onay eklendi.
PARP inhibitörlerinin en avantajlı özelliği, doğrudan kanser hücrelerini hedefleyerek kalıtsal olarak sahip oldukları eksikleri etkinliğini göstermek için kullanırken, sağlıklı hücre işleyişine az etki etmesidir. Homolog rekombinasyon onarım yolağında eksikliğe sahip tümörler, PARP inhibitörlerinin etki mekanizmalarına karşı oldukça savunmasızdırlar. Böylece inhibitörlerle etkisi baskılanan DNA tamirinde önemli bir rol oynayan PARP proteini ve sahip olduğu eksiklikler nedeni ile işlevini yerine getiremeyen HR yolağı, tümör hücrelerinin DNA’larında oluşan hasarın tamir edilmesini engelleyerek hücre ölümüne neden olur. Bu durum sıklıkla DNA tamir mekanizmasının korunmasında önemli bir role sahip proteinlerin üretilmesinde görevli BRCA geninin mutasyona uğradığı tümörlerde görülmektedir. BRCA geninde meydana gelen mutasyonlar dışındaki diğer mekanizmalar da homolog rekombinasyon onarım yolağında değişikliklere yol açarak PARP inhibitörlerinden klinik fayda sağlanmasına yardımcı olabilmektedirler.
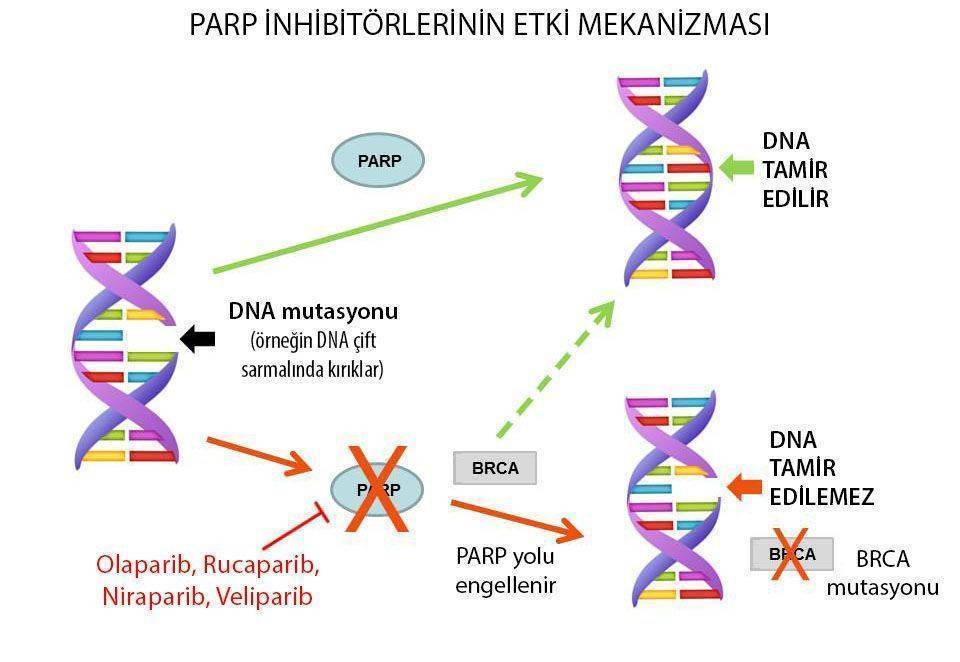
PARP, DNA’daki tek sarmal kırılmalarını onarmak için önemli olan ve hücre hasarını onarmaya yardım eden bir proteindir. BRCA1 ve/veya BRCA2 genlerinde mutasyon olması durumunda hücrelerin kendilerini onarma olasılıkları daha düşüktür. PARP inhibitörleri de DNA onarımını önleyerek hücre ölümüne yol açmaktadır.
İleri evre seröz yumurtalık kanserlerinin yaklaşık %50’si homolog rekombinasyon onarım yolağında germ hattı veya somatik mutasyon kaynaklı eksikliğe sahiptir ve bu hasta grubunun PARP inhibitörlerinden fayda sağlaması muhtemeldir. Yapılan çalışmalar göstermektedir ki, BRCA1/2 mutasyonu olan yumurtalık kanseri kadınlarda idame tedavisinde kullanılan PARP inhibitörlerinin hastalığın tekrarladığı durumlarda kullanılmaya devam etmesi, plasebo grubuna kıyasla 4 kata kadar uzun progresyonsuz sağkalım sağlamaktadır. Ayrıca, BRCA1/2 mutasyonu pozitif, birinci basamak kemoterapiye yanıt veren ve idame tedavi olarak PARP inhibitörü kullanılan hastalar plasebo grubuna kıyasla %70 daha düşük hastalık ilerlemesi ve yaşam kaybı ile karşı karşıyadırlar. Ancak, hastalığın tekrarlaması durumunda sıklıkla gözlenen platine direnç gelişmesi PAPR inhibitörlerinden yanıt almayı engellemektedir.
PARP inhibitörlerine ilişkin yeni veriler
Günümüzde PARP inhibitörlerinden sadece BRCA mutasyonu pozitif hastaların değil, tüm over kanserli hastaların fayda gördüğünü biliyoruz. Elbette, BRCA mutant ve HR eksikliği olan hastalar daha fazla fayda görmektedir, fakat BRCA mutant olmasa bile, ilk seri platin bazlı kemoterapiye iyi yanıt veren hastalar da PARP inhibitörlerinin idame tedavisinden fayda görmekteler ve Nisan 2019'da niraparib, PRIMA çalışması ile idame tedavi olarak onay almıştır.
İleri evre over kanserli hastalar için idame tedavide ilk FDA onayları iki sıra ve daha fazla tedavi alan hastalarda olmuştur. İdame tedavide onay alan ilk ilaç niraparib olmuştur (Mart 2017), daha sonra olaparib ve rucaparib sırayla onay almışlardır. Yukarıda da ifade ettiğimiz gibi, bu ilaçların başarılı bir kemoterapi sonrası idame tedavide verildiğinde hastalığın ilerlemesine kadar geçen süreyi 4 kat arttırdığı ve hastalığın tekrarlama veya ölüm riskini %70’den fazla azalttığı gösterilmiştir. Bu başarı BRCA mutasyonu olan hastalarda daha belirgin olmaktadır, ancak BRCA mutasyonu olmayan hastalarda da risk azalması %60’larda bulunmuştur.
Birinci basamak tedaviden sonra idame tedavide ise ilk onay alan PARP inhibitörü olaparib olmuştur (Aralık 2018). İlk basamak sonrası idame tedavisinde olaparib alan hastalarda tekrarlama riskini %70 azaldığı görülmüştür. Bu basamaktaki FDA onayı BRCA mutant olan hastalarda geçerlidir. Nirapribin birinci basamak tedavi sonrası idame tedavi çalışması (PRIMA) Eylül 2019’da yayınlandı; humolog rekombinasyon eksikliği olan hastalarda progresyon riskini %57 azaltmış ve progresyon süresini 2 kat uzatmıştır, FDA onayı ise 29 Nisan 2020'de gelmiştir.
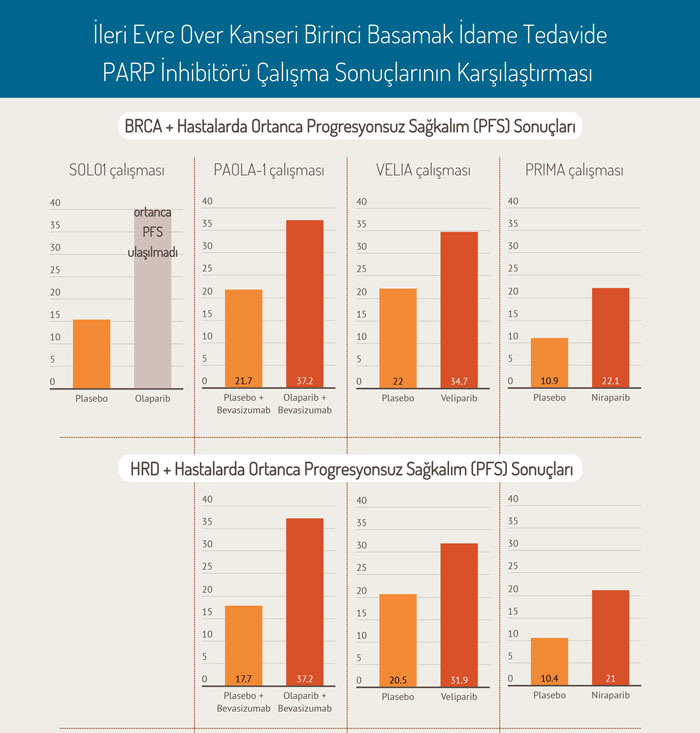
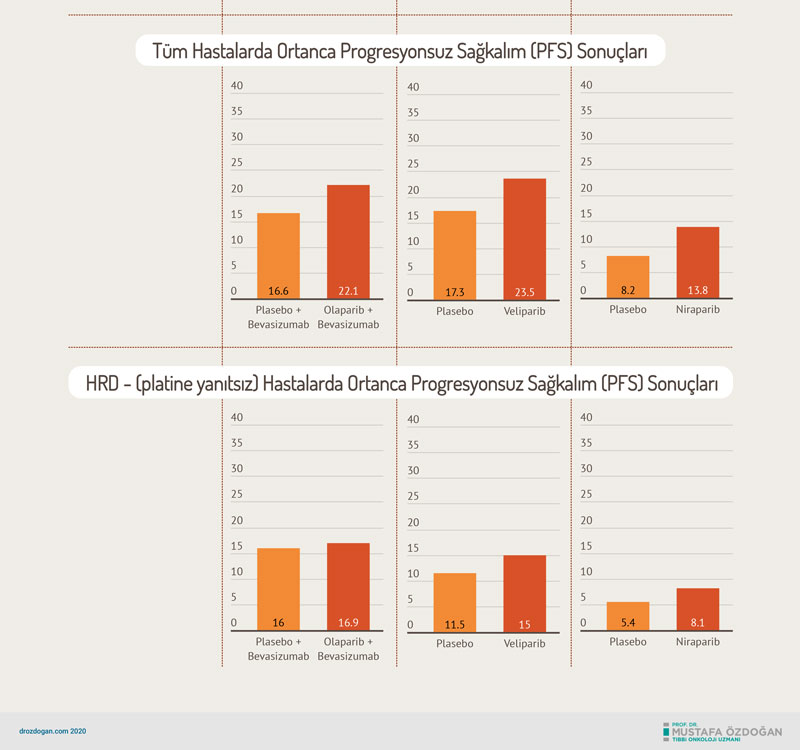
PARP inhibitörlerinin son FDA onayı ise Mayıs 2020'de, ilk kez PARP inhibitörleri ile birlikte VEGF inhibitörlerinin etkinliği ve güvenilirliğinin değerlerindirildiği PAOLA1 çalışmasıdır. Bu çalışmada olaparib artı damar önleyici ajan bevasizumab alan hasta grubu, plasebo ile bevasizumab kullanılan grup ile karşılaştırıldı. Sonuçta, PARP inhibitörünün kullanımı ile ortalama progresyonsuz sağkalım süresinin 17,7 aydan 37,2 aya uzadığı tespit edildi ve bu sonuçlarla FDA onayı aldı (bakınız ilgili onay).

Veliparib ise şimdiye kadar çok sayıda klinik araştırmada denenen, fakat henüz FDA onayı almayan bir PARP inhibitörüdür. Eylül 2019'da sonuçları yayımlanan VELIA çalışmasında bu PARP inhibitörü farklı bir şekilde kullanılmıştır: birinci basamak sistemik tedavisi sonrası değil, direkt olarak birinci basamak sistemik tedavi içinde ve sonrasında idame olarak kullanılmıştır. Yeni tanı ileri evre over kanserinde, karboplatin + paklitakselle indüksiyon kemoterapisine ek veliparib ve idame veliparib, sadece kemoterapiye kıyasla daha iyi progresyonsuz sağkalım gösterdi, fakat henüz FDA onayı almadı.
Hastaları PARP inhibitörleri hakkında bilgilendirmenin önemi
Yumurtalık kanseri olan kadınlar başlangıçta kemoterapiden hemen sonra PARP inhibitörleri ile idame tedavisine başlama konusunda tereddütlü olsalar da, tedavinin başlangıcından itibaren tüm süreçlerin anlatılması, tedavi planının tam çizilmesi ve idame tedavisi hakkında bilgilendirilmesi muhtemelen hastaları rahatlatacaktır.
Eğer bir PARP inhibitörünün idame tedavi olarak kullanılması muhtemel ise, hasta kemoterapiden sonra tedavinin bitmeyeceğini bilmelidir. Özellikle ileri evre kanserlerde yaşam süresinin kısa olduğu durumlarda, gerekli tüm bilginin hastaya doğru ve eksiz bir şekilde aktarılması son derece önemlidir.
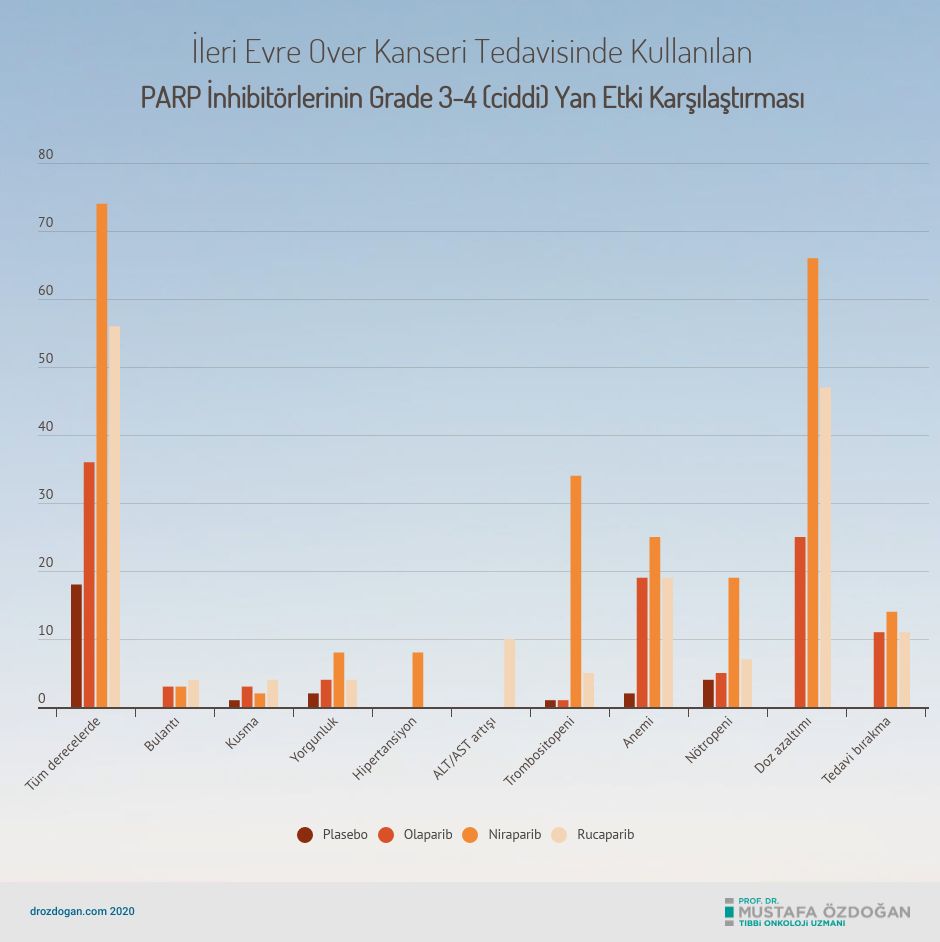
Bunun yanında hastaların PARP inhibitörlerinin olası yan etkileri hakkında da bilgilendirilmesi son derece önemlidir. Bulantı, yorgunluk ve anemi (kansızlık) kemoterapiden farklı olarak, PARP inhibitörlerinin çoğu yan etkisi tedavinin başlangıcında meydana gelmektedir. Yan etkilerin zamanlaması iyi bir şekilde açıklanmazsa, hastalar ilk 2 hafta içinde PARP inhibitörünü bırakmak isteyebilir. Pek çok hasta, mide bulantısı ve yorgunluk gibi yan etkilerin 2. haftada zirve yapması ve sonrasında azaldığı için doğru olmayan bir şekilde doz azaltımına gitmektedir. Bu nedenle, kemoterapi tamamlandıktan sonra PARP inhibitörüne başlamak için genellikle 2 ay beklemeyi tercih ediyoruz.
Sonuç
Sonuç olarak, PARP inhibitörleri artık ileri evre over kanseri tedavisinin bir standardıdır. Her ne kadar BRCA mutasyonu olanlar bu ilaçlardan daha fazla fayda görse de, BRCA mutant olmayanların da artık fayda gördüğünü biliyoruz. Son 5 yılda FDA tarafından onaylanan bu PARP inhbirötlerinin çığır açan başarılarına bakıldığında çıkarılacak olan sonuç şudur; artık her over kanserli hastada BRCA mutasyonu bakmak gerekmektedir. Ancak bu ilaçlar henüz ülkemizde onaylanmadığı için geri ödeme kapsamında kullanılamamaktadır ve kullanılmak istenmesi durumunda hasta bazında Sağlık Bakanlığı Endikasyon Dışı Onayına başvurulmalı ve onay gelmesi halinde yurtdışından ilaç temini düşünülmelidir.
Not: PARP inhibitörleri, over kanseri dışında, BRCA mutasyonlarına sahip ileri evre meme (olaparib), prostat (rucaparib) ve pankreas kanseri (olaparib) için de FDA onayı almıştır.
*






