
Meme kanseri tedavisinde son gelişmeler – CDK4/6 inhibitörlerinin ötesi
Artık etkinlikleri net olarak kanıtlanması ve ülkemizde de aktif kullanımda olmaları nedeniyle, sikline bağımlı kinaz 4 ve 6 (CDK4/6) inhibitörleri, hormon reseptörü pozitif, HER2 negatif metastatik meme kanseri tedavisinde standart bakımdır. Şimdi soru şu: CDK4/6 inhibitörü ve endokrin tedavisi ile hastalık ilerledikten sonra, bir sonraki hareket ne olmalı?
CDK4/6 sonrası
CDK4/6 inhibitörleri, hormon pozitif meme kanserli hastalar için sağkalım sonuçlarını önemli ölçüde iyileştirmiş olsa da, hastalar her zaman hastalık progresyonu yaşarlar. Edinilmiş direnç tedaviye engeldir. CDK4/6 inhibitörleri sonrası aşağıdaki seçenekler akla gelmektedir; yazıda bunları sırayla inceliyoruz:
- PI3K/AKT/mTOR hücresel sinyal yolu
- Hedeflenebilir genetik değişimleri tespitte likit biyopsi
- AKT sinyal yolu
- HER2 mutasyonu
- ESR1 mutasyonu
- Histon deasetilaz (HDAC) inhibitörleri ve BCL2 inhibitörleri
PIK3CA mutasyonlarını hedefleme
SAFIR02 adlı klinik araştırmada, hormon reseptörü-pozitif HER2-negatif metastatik meme kanserli hastaların % 28'inde PIK3CA geninin 9 veya 20. eksonlarında mutasyon saptandı. Bu hastalarda tedaviye yanıt ve stabil hastalık düşüktür; dolayısı ile daha yüksek hastalık progresyonu oranları ve daha kötü genel sağkalım gözlenmektedir [PIK3CA wilt tip (mutasyonsuz) hastalık için ortanca 23.5 aya karşı mutasyon olanlar için 19.6 ay; P = .04]. Veriler, PIK3CA mutasyonunun prognostik (hastalık gidişatını öngörücü) olduğunu gösterdi.
BOLERO-2, PI3K/AKT/mTOR yolunu hedeflemenin yararını doğrulayan ilk randomize denemeydi. Ayrıca, özellikle mTOR'u hedefleyen bir PI3K yolağı inhibitörünün onaylanmasına da yol açtı: everolimus. Tümör dokusunun veya dolaşan tümör hücresi DNA'sının (ctDNA) analizi, everolimus artı eksemestanın hem PIK3CA mutasyonlu hem de wild tip tümörlerde etkili ve plasebo ile karşılaştırıldığında yaklaşık 7 ay ve 3 ay civarında ortanca progresyonsuz sağkalım sürelerina sahip olduğunu göstermiştir. Bununla birlikte, bu verilerin daha önce bir CDK4/6 inhibitörü almamış hastalardan geldiğini not etmek önemlidir.
Daha önce bir CDK4/6 inhibitörü ile tedavi edilen hastalarda everolimusun yararını değerlendirmek, retrospektif İtalyan EVERMET çalışmasının amaçlarından biriydi. Hastalara everolimus artı eksemestan ya birinci basamak ya da ikinci basamak bir tedavi olarak verildi (ilk basamakta CDK4/6 inhibitörü veya başka bir hormon tedavisi).
İlk aşamada bu rejimle tedavi edilen hastaların en iyi progresyonsuz sağkalıma (ortanca yaklaşık 12 ay) sahip olması beklenmedik bir durum değil, ancak ilginç olan, hastaların önceki tedavisinin CDK4/6 olup olmadığına bakılmaksızın progresyonsuz sağkalımın oldukça benzer olmasıdır; inhibitör bazlı veya değil (sırasıyla yaklaşık 5 ve 7 aylık ortancalar). Bu bulgular, bir CDK4/6 inhibitörü üzerinde hastalık progresyonundan sonra everolimus kullanımına destek olduğunu gösterdi, ancak elbette bu veriler geriye dönük ve yalnızca hipotez oluşturucudur.
Onaylanacak ikinci PI3K yolu inhibitörü, alfa seçici inhibitör alpelisibdi. Alpelisibi değerlendiren temel çalışma olan SOLAR-1, mutasyon durumundan bağımsız olarak hastaları kaydetmiştir. PIK3CA mutasyonlu hasta alt grubunda, ortanca progresyonsuz sağkalım alpelisib artı fulvestrant ile 11 aya karşılık tek başına fulvestrant ile 5.7 aydı (tehlike oranı [HR] = 0.56; P = .00065); mutasyonu olmayan hastalarda hiçbir fayda gösterilmemiştir. Bu bulgu, PIK3CA mutasyon durumundan bağımsız olarak everolimusun yararının görüldüğü BOLERO-2'den biraz farklıydı.
Teşvik edici bir eğilim gösterilmesine rağmen, genel sağkalım iyileşmedi. En önemlisi, iç organ metastazlı hastalar alpelisibdeb dahah fazla fayda gördü; bu, bu yüksek riskli hastalarda alpelisib kullanımı için destek oluşturdu.
PIK3CA testi: Likit biyopsi ile mi başlamalı?
Takipteki bir hastada doku biyopsisi yapmak pratik olmadığı için, önce likit biyopsi yapıp, bu sonuç negatifse doku biyopsisi yapmak tercih edilen bir yöntemdir. Bu öneri, ctDNA'da (kanda dolaşan tümör DNA) PIK3CA tespiti ile tümör dokusu arasında uyumsuzluk bulan bir SOLAR-1 biyobelirteç analizine dayanmaktadır. Likit ctDNA wilt tip tümörlü 188 hastadan % 38'inin, daha sonra, doku tümör testi ile bir mutasyona sahip olduğu bulunmuştur ve bu hastalar alpelisibden yararlanmıştır. Bu bulgu, yalnızca ctDNA'ya güvenirsek, hastaların %40'ına kadar alpelisib tedavisini kaçırabileceğimiz anlamına gelir.
Bir CDK4/6 inhibitörü sonrasında hastalık progresyonu olan hastalarda alpelisibin etkinliğini değerlendirmek önemliydi. SOLAR-1 hasta grubunun yalnızca %6'sı bu tür hastaları içerse de, sonraki BYLieve denemesi, bir CDK4/6 inhibitöründen sonra hastalık progresyonu olan hastaların büyük bir kısmını içermiştir. Eşzamanlı verilen endokrin tedavi bir aromataz inhibitörü ise, hastalara alpelisib artı fulvestrant (kohort A); fulvestrant ise alpelisib artı letrozol (kohort B) aldılar.
Her iki grupta da birincil sonlanım noktası, 6 aylık progresyonsuz sağkalım, karşılandı. 6 ayda ilerleyici hastalığı olmadan yaşayan hastaların yüzdesi, A kohortunda %50,4 ve B kohortunda %46,1 idi; ortanca progresyonsuz sağkalım sırasıyla 7.3 ve 5.7 aydı. Kohort A, hastaların %50'sinden fazlasının 6 ayda hastalık progresyonu olmadan hayatta olduğu birincil son noktayı karşıladı.
Bulgular, bir CDK4/6 inhibitörü ile tedaviden sonra alpelisib kullanımına destek veriyor. Sonuçların, çoğu hastanın daha önce CDK inhibitörü almadığı SOLAR-1 ile güzel bir şekilde karşılaştırıldığını görmek güven verici (6 ayda hastalık progresyonu olmadan sağkalan hasta oranı %44).
Daha yeni çalışmalar, 3'lü kombinasyon ile PI3K inhibitörleri artı CDK4/6 inhibitörleri artı endokrin tedavisini denedi, ancak toksisite bu çabaları zorlaştırdı.
Diğer hedefler
Diğer çalışmalar, AKT sinyal yolağını hedeflemeyi değerlendiriyor. Randomize faz II FAKTION çalışmasında, aromataz inhibitörlerine dirençli hastalarda capivasertib artı fulvestrant tek başına fulvestrant ile karşılaştırıldı. Ortanca progresyonsuz sağkalım 10.3 aya karşılık 4.8 aydı (HR = 0.58; P = .0044) ve ortanca genel sağkalım sırasıyla 26.0'a karşı 20.0 aydı (HR = 0.59; P = .071). Bu umut verici kombinasyonun faz III CAPItello-291 denemesi şu anda devam ediyor.
Capivasertib artı paklitakselin faz I/II BEECH denemesi ve ipatasertib artı paklitaksel ile ilgili faz III IPATunity130 çalışması da dahil olmak üzere, diğer çalışmalar, AKT inhibitörünün bir endokrin ajan yerine paklitaksel ile kombine edildiğinde sonuçların o kadar iyi olmadığını göstermektedir. Her iki çalışmada da kombinasyonlar, tek başına paklitaksele göre progresyonsuz sağkalımı iyileştirmede başarısız olmuştur. Hormon reseptörü pozitif meme kanserinde AKT'yi hedefleyeceksek, muhtemelen bir endokrin partner kullanmalıyız, kemoterapi değil.
HER2 Mutasyonları
Meme kanseri denince aklımıza HER2 reseptörünün overexpresyonları gelir ve bu durum için başta trastuzumab, pertuzumab ve TDM-1 gibi oldukça etkili ilaçlar vardır. Fakat HER2'nin, overexpresyon dışı farklı değişimleri de mevcutttur: amplifikasyon ve HER2 gen mutasyonları gibi.
Aşağıda, farklı kanserlerde görülen HER2 değişiklikleri görülebilir:
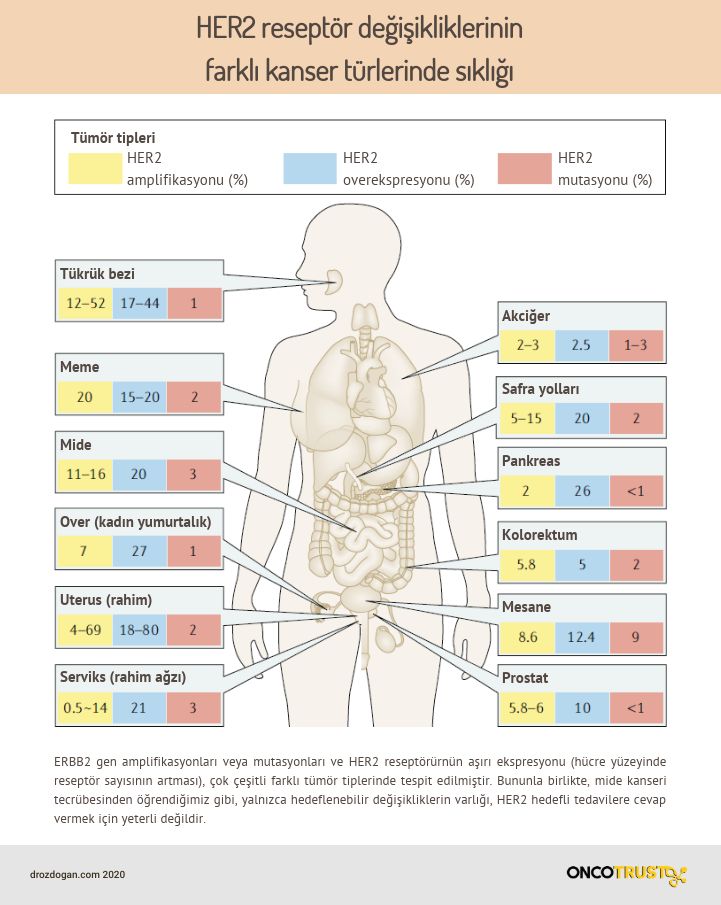
HER2 mutasyonları, östrojen reseptörü pozitif meme kanserinde de iyi bir hedef olduğunu kanıtlayabilir. SUMMIT sepet çalışmasının bir kolu, çoğunlukla daha önce fulvestrant ve bir CDK4/6 inhibitörü almış hastalarda neratinib artı trastuzumab ve fulvestrantı değerlendirdi. Yanıt oranı %46 ve ortanca progresyonsuz sağkalım 8.3 aydı ve bazı hastalarda 144 haftadan fazla remisyon görüldü. Bu çalışma, HER2 mutasyonu olan hastalarda bir tirozin kinaz inhibitörü kullanımını desteksağlıyor.
Devam eden bir faz II çalışması, HER2 mutasyonlu tümörlerde tucatinib artı trastuzumabı (ve hormon reseptörü pozitifse fulvestrant) ikinci basamak veya daha sonraki bir tedavi olarak değerlendirmektedir. Kombinasyon etkiliyse ve neratinibden daha az ishale neden oluyorsa, çalışma, HER2 mutasyonlarını daha iyi tolere edilen bir ilaçla hedefleme stratejisini doğrulayacaktır.
Aşağıda, HER2 pozitif kanserlerde kullanılan ve denenen ilaçlar listelenmiştir:
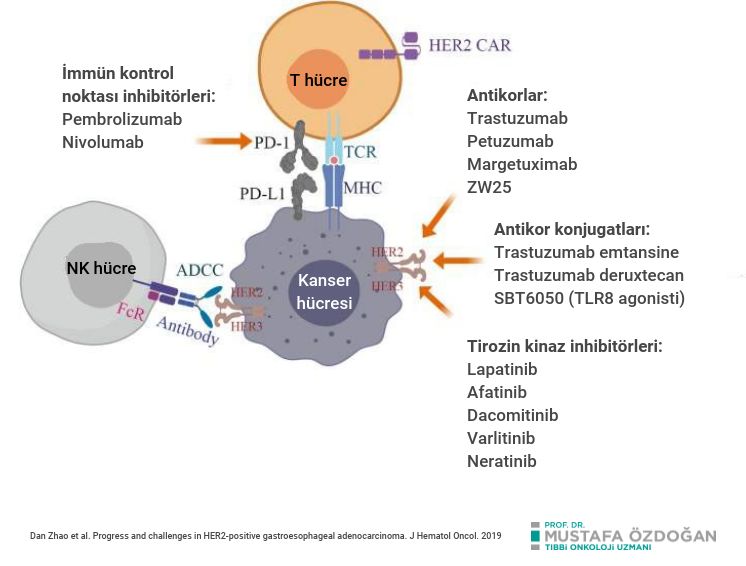
ESR1 Mutasyonları
ESR1 mutasyonları da, kanser tedavisi sırasında, kanser hücrelerinin bulduğu kaçış noktalarından biri. Tedavi ile edinilmiş gibi görünmeyen PIK3CA mutasyonlarının aksine, CDK inhibitör tedavisinden sonra ESR1 mutasyonlarının kazanıldığını görüyoruz. Birkaç denemeden elde edilen verilere göre, CDK4/6, PI3K veya mTOR inhibitörleri üzerinde ilerleyen hormon reseptörü pozitif, HER2 negatif hastalığı olan hastaların dörtte birinden fazlasında ESR1 mutasyonları gözlenir.
Birinci basamakta bir aromataz inhibitörü artı palbosiklib ile tedavi edilen 1.017 hastayı içeren faz III PRADA-1 çalışması, bu mutasyonların nasıl elde edilebileceğini ve etkili olduğunda tedavinin bunları nasıl temizleyebileceğini gösterdi. Hastalara kayıt sırasında ve tedavi sırasında ESR1 mutasyonları için hücresiz DNA testi uygulandı. Başlangıçta, hastaların %3'ünde bir ESR1 mutasyonu vardı, ancak bu durum prognozu etkiledi: mutasyonu olanlar için ortanca progresyonsuz sağkalımları 11.0 aydı ve mutasyonları olmayan hastalar için 26.7 aydı (HR = 2.3; P< .001). İlginç bir şekilde, bu mutasyonları tedavi sürecinde erkenden kaybolan hastalar için, ortanca progresyonsuz sağkalım, wilt tipteki muadillerine rakip olarak 24,1 aya yükseldi. PRADA-1, bir ESR1 mutasyonu geliştiren ancak henüz hastalık progresyonu geçirmemiş hastalar için endokrin ajanın fulvestranta geçişinin etkisini değerlendirmektedir.
Diğer yeni yaklaşımlar
Birçok farklı ilaç adayı, oral selektif östrojen reseptör baskılayıcıları olarak değerlendirilmektedir. Ek olarak, histon deasetilaz (HDAC) inhibitörleri ve BCL2 inhibitörleri de dahil olmak üzere birçok dikkat çekici deneme mevcuttur.
HDAC inhibitörü entinostatın hayal kırıklığı yarattığı kanıtlanmış olsa da, yakın zamanda tucidinostat için olumlu sonuçlar bildirilmiştir. Ayrıca, bazı kan kanserlerinde etkili olan BCL2 inhibitörü venetoclax ile görülen erken sonuçlar cesaret vericidir. BCL2, primer östrojen reseptörü pozitif tümörlerin %80'inden fazlasında aşırı eksprese edilen anti-apoptotik bir proteindir.
Bir faz Ib çalışmasında venetoclax artı tamoksifen, daha önce tamoksifen, CDK4/6 inhibitörleri veya everolimus (artı endokrin tedavisi) ile tedavi edilen hastalarda %62 ila %100'lük klinik fayda oranlarına yol açmıştır. Devam eden faz II VERONICA çalışması, CDK4/6 inhibitör tedavisinden sonra venetoklaks artı fulvestrantı değerlendirecek ve hastaları yüksek ve düşük BCL2 ekspresyonuna göre sınıflandıracaktır.
Sacituzumab govitecan-hziy gibi antikor-ilaç konjugatları ve immünoterapi ve fibroblast büyüme faktörü inhibitörlerini içeren kombinasyonlar da klinik deneylerde değerlendirilmektedir.
*
Bonus içerik: Meme kanseri tedavileri daha iyi anlamak için hazırladığımız infografik poster
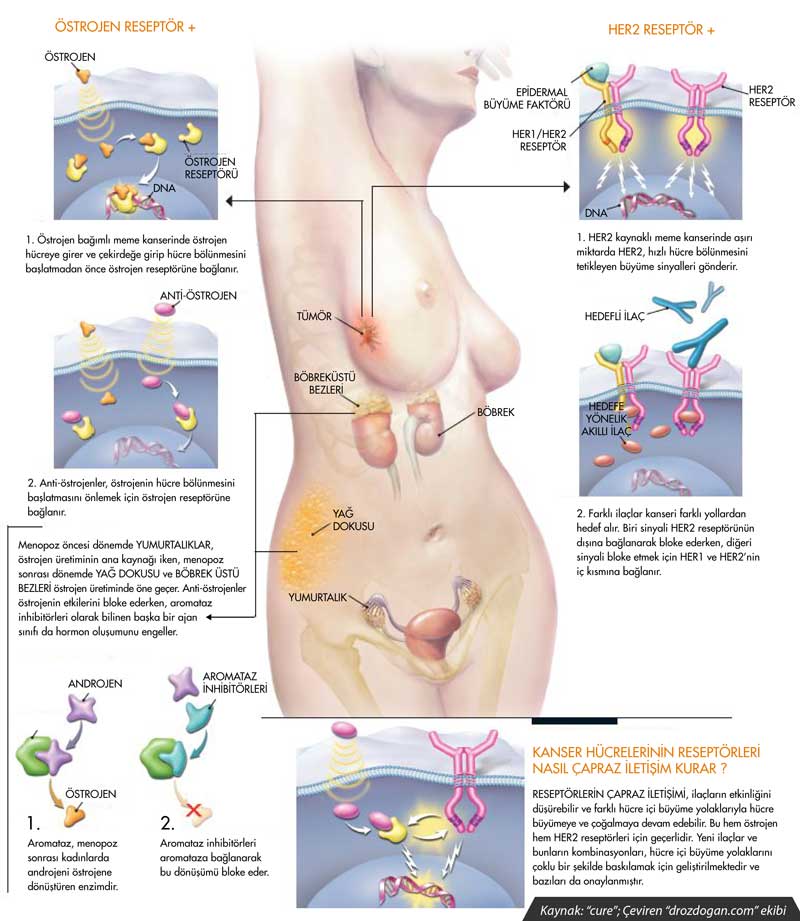
1. Hurvitz S: Metastatic ER+ breast cancer: Beyond CDK4/6 inhibition. 2021 Miami Breast Cancer Conference. Presented March 5, 2021.
2. Mosele F, Stefanovska B, Lusque A, et al: Outcome and molecular landscape of patients with PIK3CA-mutated metastatic breast cancer. Ann Oncol 31:377-386, 2020.
3. Hortobagyi GN, Chen D, Piccart M, et al:Correlative analysis of genetic alterations and everolimus benefit in hormone receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer: Results from BOLERO-2. J Clin Oncol 34:419-426, 2016.
4. Moynahan ME, Chen D, He W, et al: Correlation between PIK3CA mutations in cell-free DNA and everolimus efficacy in HR+, HER2- advanced breast cancer: Results from BOLERO-2. Br J Cancer 116:726-730, 2017.
5. Nichetti F, Marra A, Giorgi CA, et al: Efficacy of everolimus plus exemestane in CDK 4/6 inhibitors-pretreated or naive HR-positive/HER2-negative breast cancer patients: A secondary analysis of the EVERMET study. ESMO Virtual Congress 2020. Abstract 337P. Presented September 17, 2020.
6. André F, Ciruelos EM, Juric D, et al: Alpelisib plus fulvestrant for PIK3CA-mutated, hormone receptor-positive, human epidermal growth factor receptor-2-negative advanced breast cancer: Final overall survival results from SOLAR-1. Ann Oncol 32:208-217, 2021.
7. Andre F, Ciruelos E, Rubovszky G, et al: Overall survival results from SOLAR-1, a phase III study of alpelisib plus fulvestrant for hormone receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer. ESMO Virtual Congress 2020. Abstract LBA18. Presented September 19, 2020.
8. Ciruelos EM, Loibl S, Mayer IA, et al: Clinical outcomes of alpelisib plus fulvestrant in hormone receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer with PIK3CA alterations detected in plasma ctDNA by next-generation sequencing: Biomarker analysis from the SOLAR-1 study. 2020 San Antonio Breast Cancer Symposium. Abstract PD2-06. Presented December 9, 2020.
9. Rugo HS, Lerebours F, Ciruelos E, et al: Alpelisib + fulvestrant in patients with PIK3CA-mutated hormone receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer previously treated with cyclin-dependent kinase 4/6 inhibitor + aromatase inhibitor: BYLieve study results. ASCO20 Virtual Scientific Program. Abstract 1006. Presented May 29, 2020.
10. Rugo HS, Lerebours F, Juric D, et al: Alpelisib + letrozole in patients with PIK3CA-mutated, hormone-receptor positive, human epidermal growth factor receptor-2-negative advanced breast cancer previously treated with a cyclin-dependent kinase 4/6 inhibitor + fulvestrant: BYLieve study results. 2020 San Antonio Breast Cancer Symposium. Abstract PD2-07. Presented December 9, 2020.
11. Jones RH, Casbard A, Carucci M, et al: Fulvestrant plus capivasertib versus placebo after relapse or progression on an aromatase inhibitor in metastatic, oestrogen receptor-positive breast cancer (FAKTION): A multicentre, randomized, controlled, phase 2 trial. Lancet Oncol 21:345-357, 2020.
12. Turner NC, Alarcón E, Armstrong AC, et al: BEECH: A dose-finding run-in followed by a randomised phase II study assessing the efficacy of AKT inhibitor capivasertib (AZD5363) combined with paclitaxel in patients with estrogen receptor-positive advanced or metastatic breast cancer, and in a PIK3CA mutant sub-population. Ann Oncol 30:774-780, 2019.
13. Turner N, Dent R, O’Shaughnessy J, et al: Ipatasertib + paclitaxel for PIK3CA/AKT1/PTEN-altered hormone receptor-positive HER2-negative advanced breast cancer: Primary results from Cohort B of the IPATunity130 randomised phase III trial. ESMO Virtual Congress 2020. Abstract 283MO. Presented September 18, 2020.
14. Jhaveri K, Saura C, Guerrero-Zotano A, et al: Latest findings from the breast cancer cohort in SUMMIT: A phase 2 ‘basket’ trial of neratinib + trastuzumab + fulvestrant for HER2-mutant, hormone receptor-positive, metastatic breast cancer. 2020 San Antonio Breast Cancer Symposium. Abstract PD1-05. Presented December 9, 2020.
15. Bidard FC, Callens C, Dalenc F, et al: Prognostic impact of ESR1 mutations in ER+ HER2- MBC patients with prior treatment with first-line AI and palbociclib: An exploratory analysis of the PRADA-1 trial. ASCO20 Virtual Scientific Program. Abstract 1010. Presented May 30, 2020.
16. Jiang Z, Li W, Hu X, et al: Tucidinostat plus exemestane for postmenopausal patients with advanced, hormone receptor-positive breast cancer (ACE): A randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol 20:806-815, 2019.
17. Lok SW, Whittle JR, Vaillant F, et al: A phase Ib dose-escalation and expansion study of the BCL2 inhibitor venetoclax combined with tamoxifen in ER and BCL2-positive metastatic breast cancer. Cancer Discov 9:354-369, 2019.






