
Ribosiklib (Valamor) Nedir? FDA Onayı, Türkiye Ruhsatı ve Geri Ödeme Durumu
Valamor (Ribosiklib) Künyesi
- İlk FDA Onayı: 2017
- Kutu Adı: Valamor (Türkiye), Kisqali (ABD)
- Etken Madde Adı: Ribosiklib
- Uygulama Şekli: Ağız yoluyla alınır (oral).
- Sınıfı: Sinyal transdüksiyon inhibitörü, CDK (Cyclin-dependent kinase) inhibitörü.
- Kategori: Hedefe yönelik ajan (Targeted agent)
- Üretici: Novartis
- Türkiye Dağıtımı: Novartis
- Onaylı Olduğu Kanserler:
- Hormon reseptörü (HR) pozitif, HER2-negatif yüksek riskli erken evre meme kanseri
- Hormon reseptörü (HR) pozitif, HER2-negatif metastatik meme kanseri
Valamor Nedir? Ne İşe Yarar ve Nasıl Etki Eder?
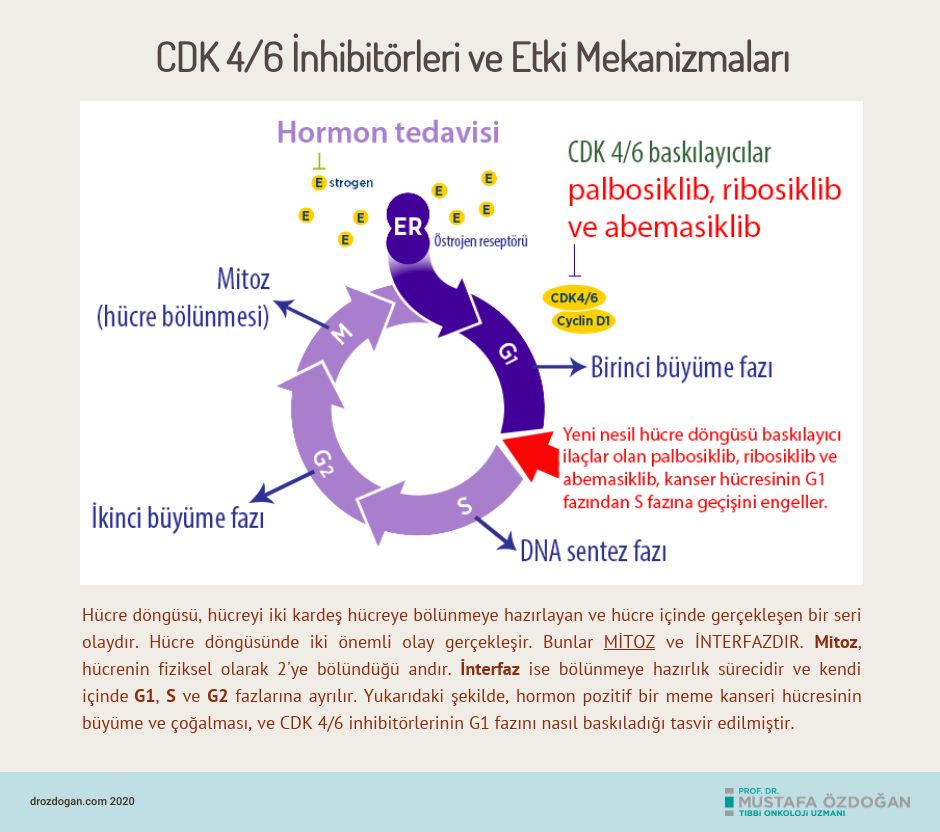
Valamor (etken maddesi ribosiklib), hormon reseptörü pozitif meme kanseri olan hastaları tedavi etmek için klasik hormon baskılayıcı ilaçlar ile birlikte kullanılabilen yeni nesil kanser ilaçlarından biridir. Valamor, küçük moleküllü bir sikline bağımlı kinaz (CDK) inhibitörüdür. İlaç, hücrede sikline bağımlı kinaz (CDK) 4 ve CDK 6 adı verilen proteinleri bloke eder.
Hormon pozitif meme kanseri hücrelerinde, bu proteinlerin bloke edilmesi, hücrelerin yeni hücreler oluşturmak için bölünmesini durdurmaya yardımcı olur. Bölünme sürecinde hücrelerin G1'den S hücre döngüsü aşamasına geçmesini önlemeye yardımcı olur. Bu, kanser büyümesini yavaşlatır. Valamor ve bir aromataz inhibitörünün (örneğin letrozol, anastrazol) veya seçici östrojen downregülatörünün (fulvestrant) kombinasyonu, tek başına kullanıma göre daha etkilidir.
Hedefe yönelik akıllı kanser tedavileri, kanser hücreleri ile normal hücreler arasındaki farkları anlamaya adanmış yaklaşık 100 yıllık araştırmanın sonucudur. Bugüne kadar kanser tedavisi, öncelikle hızla bölünen hücreleri öldürmeye odaklanmıştı. Çünkü kanser hücrelerinin bir özelliği, hızlı bölünmeleridir. Ne yazık ki, bazı normal hücrelerimiz de hızla bölünmektedir, bu yüzden kemoterapilere bağlı birden çok yan etki oluşmaktadır. Hedefe yönelik tedavi, kanser hücrelerinin diğer özelliklerini tanımlamakla ilgilidir. Bilim insanları, kanser hücrelerinde ve normal hücrelerde belirli farklılıklar ararlar. Bu bilgi, normal hücrelere zarar vermeden kanser hücrelerine saldırmak için hedefli bir tedavi oluşturmak için kullanılır. Böylece daha az yan etkiye yol açar.
FDA (ABD Gıda ve İlaç İdaresi) Onay Tarihçesi
Ribosiklib etken maddeli Valamor'un FDA onay tarihleri ve endikasyonları aşağıdaki gibidir:
- Mart 2017: İleri evre hormon pozitif HER2 negatif postmenopozal meme kanserli kadınlarda, aromataz inhibitörü (Aİ) ile birlikte 1. basamakta onay aldı.
- Temmuz 2018: İleri evre hormon pozitif HER2 negatif hem premenopozal hem perimenopozal hem de postmenopozal ileri evre hastalarda Aİ ile birlikte 1. basamakta onay aldı. Ayrıca postmenopozal hastalarda fulvestrant ile birlikte 1. veya 2. basamakta onay aldı.
- Eylül 2024: Hormon reseptörü (HR) pozitif, insan epidermal büyüme faktörü reseptörü 2 (HER2) negatif, nüks riski yüksek evre 2 ve 3 meme kanserinin adjuvan tedavisi için ribosiklibin aromataz inhibitörü ile birlikte kullanımını onayladı.
Türkiye Ruhsatı
Valamor, T.C. Sağlık Bakanlığı tarafından şu endikasyonlar için ruhsatlandırılmıştır:
- VALAMOR + NSAİ: NSAİ (nonsteroidal aromataz inhibitörü) ile kombine kullanımı halinde; östrojen reseptörü (ER) en az %10 pozitif, HER2 negatif pre/peri/postmenopozal metastatik meme kanseri olan, daha önce metastatik hastalık için endokrin tedavi almış hastalar ile birlikte adjuvan NSAİ tedavisinin tamamlanmasından 12 ay sonra relaps yapmış veya adjuvan tamoksifen tedavisi sırasında veya sonrasında relaps yapmış hastalarda endikedir.
- VALAMOR + Fulvestrant: Östrojen reseptörü (ER) en az %10 pozitif ve HER2 (-) olan pre/peri/postmenopozal metastatik meme kanserli, daha önce fulvestrant kullanmamış hastalarda:
- Metastatik hastalık tedavisi için ilk sıra ve en az 6 ay aromataz inhibitörü alırken klinik veya radyolojik hastalık progresyonu görülenlerde fulvestrant ile birlikte kullanılır.
- Adjuvan aromataz inhibitörü tedavisini 12 ay ve süreyle kullandıktan sonra ya da adjuvan aromataz inhibitörü tedavisini tamamladıktan sonraki 12 ay içinde nüks/metastaz yapmış hastalarda fulvestrant ile birlikte kullanılır.
- Daha önce fulvestrant kullanmış metastatik hastalarda metastatik hastalık tedavisinin ilk sırasında NSAİ kullanımı önerilir. Bu hastalarda daha sonra endokrin tedavisi almamış olan hastalarda kullanılamaz.
- Pre/perimenopozal kadınlarda endokrin tedavisi, luteinizan edici hormon salgılatıcı hormon (LHRH) agonisti ile birleştirilmelidir.
Geri Ödemesi Var mı?
Valamor Türkiye'de SGK tarafından aşağıdaki durumlarda geri ödenmektedir:
- NSAİ ile kombine kullanımda: ER %10+, HER-2 (-) pre/peri/postmenopozal metastatik meme kanseri olan, daha önce metastatik hastalık için endokrin tedavi almamış hastalar veya adjuvan NSAI tedavisinin tamamlanmasından 12 ay sonra relaps yapmış veya adjuvan tamoksifen tedavisi sırasında/sonrasında relaps yapmış hastalarda en fazla 6 ay süreli sağlık kurulu raporuna istinaden ödenir.
- Fulvestrant ile kombine kullanımda: Daha önce fulvestrant kullanmamış hastalarda:
a) Metastatik tedavi için bir sıra ve en az 6 ay Aİ kullandıktan sonra progresyon görülenlerde.
b) Adjuvan Aİ tedavisi devam ederken (en az 12 ay almış olmak şartıyla) veya tamamlandıktan sonraki 12 ay içinde nüks gelişen hastalarda.
Fiyatı: Mart 2026 itibarıyla Valamor 200 mg 63 tablet eczane satış fiyatı ve bir kürlük maliyeti 67.864,35 TL'dir.
*Rapor süresinin sonunda tedavinin devamı için düzenlenecek yeni raporda hastalık progresyonu olmadığı belirtilmelidir.
Direnç Mekanizması
- CDK6'nın aşırı ekspresyonu veya CDK2'nin artmış ifadesi
- pRb proteininin kaybı
- Cyclin A ve E'nin aşırı üretimi
Farmakokinetik Bilgiler
| Emilim | Oral biyoyararlanım %46'dır. Doruk plazma düzeylerine 1-4 saatte ulaşılır. Gıdanın emilim üzerinde belirgin bir etkisi yoktur. |
| Dağılım | Plazma proteinlerine yaklaşık %70 oranında bağlanır. Kararlı durum plazma seviyeleri yaklaşık 8 gün içinde elde edilir. |
| Metabolizma | Esas olarak karaciğerde CYP3A4 enzimleri tarafından metabolize edilir. %70'i feçes yoluyla, %23'ü idrarla atılır. |
Doz Aralığı
- Başlangıç dozu: Aralıksız 21 gün boyunca günlük 600 mg (3 tane 200 mg tablet), ardından 7 gün ilaç kullanmaya ara verilir (1 kür).
- Tedavi, artık işe yaramayana veya kabul edilemez yan etkiler yaşanana kadar sürdürülür. Her kür 28 günde bir tekrarlanır.
İlaç Etkileşimleri
- CYP3A4 Uyarıcılar: (Fenitoin, karbamazepin, rifampin vb.) Plazma düzeylerini düşürebilir.
- CYP3A4 İnhibitörleri: (Ketokonazol, itrakonazol vb.) Plazma düzeylerini artırarak toksisite riskini yükseltebilir.
- QT Uzaması: Kalp ritmini bozan ilaçlarla kombinasyondan kaçınılmalıdır.
Dikkat Edilmesi Gereken Durumlar
- Yiyecekle veya aç karnına alınabilir. Tableti bütün yutun; çiğnemeyin, ezmeyin veya kırmayın.
- Doz atlarsanız telafi etmeyin, sonraki dozu planlandığı gibi ertesi gün alın.
- Beslenme Kısıtlaması: Nar, greyfurt, yıldız meyvesi, kan portakalı ve sularından kaçının (ilacın kan seviyesini artırabilir). Limon ve misket limonu tüketilebilir.
- Sarı Kantaron: Kullanmaktan kaçının (etkinliği azaltabilir).
- Oda sıcaklığında orijinal ambalajında saklayın. Blisterden kullanana kadar çıkarmayın.
- Kalp ritmini bozduğu bilinen ilaçlarla etkileşime girebilir; eczacınızdan kontrol etmesini isteyin.
- Hamilelik/Emzirme: Fetüse zarar verebilir. Tedavi sırasında ve son dozdan sonra en az 3 hafta boyunca etkili doğum kontrolü kullanılmalı ve emzirilmemelidir.
Yan Etkiler
Yaygın Yan Etkiler (%30'dan fazla):
- Düşük kan sayımı (lökopeni, nötropeni, anemi, trombositopeni); enfeksiyon ve kanama riski.
- Mide bulantısı, kusma, ishal ve yorgunluk.
- Karaciğer enzimlerinde (ALT ve AST) artış.
- Saç kaybı.
Daha Az Yaygın Yan Etkiler (%10-29):
Kabızlık, baş ağrısı, sırt ağrısı, böbrek fonksiyonunda azalma (kreatinin yükselmesi), iştah kaybı, döküntü, ateş, kaşıntı, ödem, uykusuzluk, ağız yaraları ve idrar yolu enfeksiyonu.
Takip
Kan Testleri: İlk 2 kür için 2 haftada bir, sonra her kür başında Hemogram ve Biyokimya kontrol edilir.
Görüntüleme: Tedavi öncesi ve periyodik olarak BT, MRG veya PET-BT önerilir.
Kardiyoloji: Tedavi öncesi, 2. hafta ve 2. kür başında EKG çekilir.
Kemik Sağlığı: Kemik gücünü izlemek için DEXA taramaları yapılabilir.
1. Slamon DJ, Neven P, Chia S, et al. Phase III Randomized Study of Ribociclib and Fulvestrant in Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Advanced Breast Cancer: MONALEESA-3. J Clin Oncol. 2018
2. Hortobagyi GN, Stemmer SM, Burris HA, et al. Ribociclib as First-Line Therapy for HR-Positive, Advanced Breast Cancer. N Engl J Med. 2016






